Περίληψη των σημαντικότερων στοιχείων των μελετών
Αύγουστος 2022
Επιμέλεια
Επιστημονική πρωτοβουλία «Υγεία για την Αυστρία»

Επιπλέον πληροφορίες και στοιχεία απο Ελλάδα
Επιστήμονες για την Υγεία και την Ελευθερία

*Στο τέλος της δημοσίευσης μπορείτε να βρείτε τη συγκεκριμένη έρευνα σε μορφή PDF.
Περιεχόμενα
2-Στόχος της παρούσας ανάλυσης.
3-Πόσο επικίνδυνη είναι η COVID;
4-Προστασία του εμβολιασμού από συμπτωματική λοίμωξη, σοβαρή πορεία και θάνατο.
4.1-Προστασία μέσω της βασικής ανοσοποίησης κατά της συμπτωματικής λοίμωξης.
4.3-Αποτελεσματικότητα των αναμνηστικών εμβολιασμών.
4.4-Διάρκεια της προστασίας από τους εμβολιασμούς COVID.
4.5-Αποτελεσματικότητα των διαθέσιμων εμβολίων κατά των μεταλλάξεων του SARS-CoV-2.
4.6-Αποτελεσματικότητα του εμβολίου σε παιδιά και εφήβους.
4.8-Επιδράσεις του εμβολιασμού στη Long COVID.
4.9- Προστασία από τη μολυσματικότητα και στείρα ανοσία.
5- Παρενέργειες των εμβολιασμών COVID.
5.1-Παρενέργειες στις μελέτες καταχώρισης.
5.3-Δεδομένα φαρμακοεπαγρύπνησης των κατασκευαστών.
5.5-Ειδικές παρενέργειες εμβολιασμού των εμβολίων COVID και των Red Hand Letters.
5.7-Υπερβολική θνησιμότητα που σχετίζεται με τους εμβολιασμούς COVID.
5.8-Αποβολές και μειωμένη γονιμότητα.
6-Σχέση κινδύνου-οφέλους των εμβολιασμών COVID.
7. Ενδείξεις εμβολιασμών COVID με δυνητικά ευνοϊκή σχέση κινδύνου-οφέλους.
8. Αντενδείξεις για τον εμβολιασμό COVID λόγω πιθανής αρνητικής σχέσης κινδύνου-οφέλους.
9- Αξιολόγηση των διαθέσιμων στοιχείων των μελετών σύμφωνα με το GRADE.
10-Ενημερωτική και συμμετοχική λήψη αποφάσεων για τον εμβολιασμό με βάση την τεκμηρίωση.
1-Περίληψη
Όσον αφορά τον συνολικό πληθυσμό, η COVID-19 είναι ασήμαντα πιο επικίνδυνη από τη μέση εποχική γρίπη, με μέσο ποσοστό θνησιμότητας λόγω λοίμωξης (IFR) περίπου 0,1 έως 0,2%. Ωστόσο, σε αντίθεση με τη τελευταία, προσβάλλονται σχεδόν αποκλειστικά άτομα με προϋπάρχουσες ασθένειες σε μεγαλύτερη ηλικία. Σε αντίθεση με τη γρίπη, τα παιδιά επηρεάζονται ελάχιστα από την COVID. Συνεπώς, η ανάλυση κινδύνου-οφέλους για τον εμβολιασμό κατά της COVID πρέπει να λαμβάνει υπόψη ότι υπάρχει ελάχιστος κίνδυνος σοβαρής νόσου για νέους και υγιείς ανθρώπους.
Αξιόπιστα στοιχεία μελετών για την αποτελεσματικότητα των εμβολίων COVID από τυχαιοποιημένες ελεγχόμενες μελέτες (καταγραφής) υπάρχουν μόνο για τις πρώτες έξι έως οκτώ εβδομάδες μετά τον ολοκληρωμένο εμβολιασμό και περιορίζονται σε ήπιες, θετικές στη δοκιμασία PCR, συμπτωματικές ασθένειες. Από τις τυχαιοποιημένες ελεγχόμενες δοκιμές δεν μπορεί να προκύψει επίδραση κατά των σοβαρής νόσου ή του θανάτου λόγω COVID. Η αξιολόγηση μετά από έξι μήνες για το εμβόλιο Comirnaty® της Pfizer/BioNTech δεν δείχνει καμία διαφορά στη συνολική θνησιμότητα μεταξύ της ομάδας εμβολιασμένων και της ομάδας εικονικού φαρμάκου (placebo). Για τα άλλα εμβόλια δεν υπάρχουν παρατηρήσεις παρακολούθησης από τις τυχαιοποιημένες ελεγχόμενες δοκιμές.
Τα αποδεικτικά στοιχεία για την πρόληψη της σοβαρής νόσου COVID και των θανάτων από COVID βασίζονται αποκλειστικά σε αναδρομικές μελέτες παρατήρησης και μελέτες ελέγχου περιπτώσεων, οι οποίες έχουν σοβαρές μεθοδολογικές ατέλειες και, ως εκ τούτου, χαμηλό έως πολύ χαμηλό επίπεδο αποδεικτικών στοιχείων. Αυτό ισχύει τόσο για τις μελέτες που διερευνούν τον βασικό εμβολιασμό όσο και για εκείνες που μετρούν την αποτελεσματικότητα του αναμνηστικού εμβολιασμού. Έτσι, σε αυτές τις μελέτες αξιολογούνται μόνο τα συμβάντα που συνέβησαν μία έως δύο εβδομάδες μετά τον πλήρη εμβολιασμό (ή μετά την αναμνηστική δόση). Εξαιρώντας το χρονικό διάστημα μεταξύ του πρώτου εμβολιασμού ή αναμνηστικού εμβολίου και της έναρξης της καταμέτρησης των συμβάντων, το αποτέλεσμα μπορεί να είναι μεροληπτικό υπέρ του εμβολιασμού, επειδή δεν υπολογίζονται οι νοσηλείες και οι θάνατοι που σχετίζονται με τον εμβολιασμό. Επιπλέον, αναφέρονται μόνο οι νοσηλείες και οι θάνατοι που σχετίζονται με COVID, αλλά όχι το συνολικό ποσοστό νοσηλείας και η συνολική θνησιμότητα. Αυτό οδηγεί επίσης σε μεροληψία υπέρ του εμβολιασμού, επειδή δεν λαμβάνονται υπόψη τα συμβάντα που οφείλονται σε παρενέργειες του εμβολιασμού και απουσιάζει η αναφορά σε απόλυτους αριθμούς. Δεδομένου ότι στις μελέτες χρησιμοποιούνται δεδομένα από τα ασφαλιστικά ταμεία, είναι ασφαλές να υποθέσουμε ότι οι συγγραφείς γνώριζαν το συνολικό ποσοστό νοσηλείας και τη συνολική θνησιμότητα ή θα μπορούσαν εύκολα να τα προσδιορίσουν. Το γεγονός ότι αυτά δεν αναφέρονται εγείρει την υποψία ότι αποκρύφθηκαν σκόπιμα, ενδεχομένως λόγω των πολυάριθμων συγκρούσεων συμφερόντων των περισσότερων συγγραφέων. Όλες οι μελέτες παρακολούθησης έχουν επίσης πολύ σύντομες περιόδους παρατήρησης (λίγες εβδομάδες), έτσι ώστε να μην μπορούν να εξαχθούν συμπεράσματα σχετικά με τη μακροπρόθεσμη αποτελεσματικότητα του εμβολιασμού.
Λίγες μακροχρόνιες μελέτες παρατήρησης δείχνουν ότι η όποια αποτελεσματικότητα του εμβολίου μπορεί να υπάρχει αρχικά, μειώνεται γρήγορα και χάνει τη δράση του μετά από έξι έως εννέα μήνες. Είναι πιθανό η ανοσία του εμβολίου να αποκατασταθεί βραχυπρόθεσμα με τον αναμνηστικό εμβολιασμό (booster), αλλά χάνεται εξίσου γρήγορα. Επιπλέον, παρατηρείται σημαντική μείωση της αποτελεσματικότητας του εμβολίου έναντι των νέων παραλλαγών του SARS-CoV-2. Μια σχετική αποτελεσματικότητα του εμβολίου κατά της παραλλαγής Omikron είναι πολύ απίθανη.
Οι μελέτες σχετικά με την αποτελεσματικότητα του εμβολιασμού σε παιδιά και εφήβους είναι σαφώς περιορισμένες σε σύγκριση με τις μελέτες σε ενήλικες. Είναι σε μεγάλο βαθμό άγνωστο κατά πόσον ο εμβολιασμός προλαμβάνει τις σοβαρές νόσους και τους θανάτους σε αυτή την ηλικιακή ομάδα, καθώς αυτά είναι ούτως ή άλλως εξαιρετικά σπάνια στα παιδιά και τους εφήβους.
Σύμφωνα με τις τρέχουσες μελέτες, τα άτομα που έχουν αναρρώσει δεν ωφελούνται από τον πρόσθετο εμβολιασμό όσον αφορά το ποσοστό της νόσου. Ο κίνδυνος σοβαρής νόσου ή θανάτου από την COVID είναι πολύ χαμηλός για όσους έχουν αναρρώσει. Μία πρόσφατη μελέτη από το Κατάρ επιβεβαιώνει ότι Η αποτελεσματικότητα έναντι σοβαρής ασθένειας με τη φυσική ανοσία είναι 84,6% [102]. Δεν υπάρχει καμία μελέτη που να αποδεικνύει ότι ο εμβολιασμός είναι επωφελής από αυτή την άποψη.
Το κατά πόσον ο εμβολιασμός προστατεύει από τη long-COVID δεν έχει ακόμη διερευνηθεί σε μελέτες επαρκούς ποιότητας. Μια μικρή θετική επίδραση φαίνεται πιθανή, αλλά είναι άγνωστο πόσο διαρκεί αυτή η επίδραση και αν υπάρχουν μακροπρόθεσμες διαφορές στην αυθόρμητη πορεία της long-COVID.
Έχει πλέον αποδειχθεί με ασφάλεια ότι η στείρα ανοσία δεν επιτυγχάνεται με κανένα από τα διαθέσιμα εμβόλια COVID. Αντιθέτως, μελέτες δείχνουν ότι το ιικό φορτίο εμβολιασμένων και μη εμβολιασμένων ατόμων με συμπτωματική νόσο COVID είναι το ίδιο και ότι μπορούν να μολύνουν εξίσου άλλα εμβολιασμένα και μη εμβολιασμένα άτομα. Συνεπώς, ο εμβολιασμός δεν εμποδίζει την εξάπλωση του ιού και δεν συμβάλλει στην ανάπτυξη της λεγόμενης ανοσίας αγέλης.
Όλα τα εμβόλια COVID που χρησιμοποιούνται ευρέως μέχρι σήμερα (δηλαδή τα εμβόλια mRNA και τα εμβόλια ιικών φορέων- δεν υπάρχουν ακόμη επαρκή στοιχεία για το πρόσφατα εγκεκριμένο αδρανοποιημένο εμβόλιο με βάση την πρωτεΐνη) έχουν ανησυχητικό προφίλ παρενεργειών. Οι σημαντικότερες σοβαρές παρενέργειες περιλαμβάνουν μυοκαρδίτιδα, περικαρδίτιδα, θρομβοεμβολικά επεισόδια, νευρολογικές και αυτοανοσολογικές παθήσεις, ορισμένες από τις οποίες είναι θανατηφόρες. Σύμφωνα με εκτιμήσεις που βασίζονται στις εκθέσεις ασφάλειας του Ινστιτούτου Paul Ehrlich και στην ευρωπαϊκή βάση δεδομένων αναφερόμενων ύποπτων ανεπιθύμητων ενεργειών EudraVigilance, το ποσοστό αναφοράς ανεπιθύμητων ενεργειών είναι 60 φορές υψηλότερο(20/100.000 δόσεις εμβολίου) και το ποσοστό αναφοράς θανάτων είναι 20 φορές υψηλότερο (1,6/100.000 δόσεις εμβολίου) σε σύγκριση με όλα τα άλλα συμβατικά εμβόλια. Υπάρχει επίσης η υποψία της έλλειψης υποβολής αναφορών κατά τουλάχιστον 10 φορές.
Υπάρχει μεγάλη πιθανότητα αρνητικής σχέσης κινδύνου-οφέλους για όλα τα εμβόλια COVID για νέους και υγιείς ανθρώπους, ιδίως για παιδιά και εφήβους. Οι υγιείς ηλικιωμένοι είναι επίσης πολύ απίθανο να ωφεληθούν από τον εμβολιασμό. Χρησιμοποιώντας το σύστημα GRADE για την αξιολόγηση της τεκμηρίωσης των μελετών και της ισχύος της σύστασης, στην καλύτερη περίπτωση μπορεί να γίνει μια ασθενής σύσταση για εμβολιασμό για ηλικιωμένους με συνοδά νοσήματα, ιδίως σακχαρώδη διαβήτη, καρδιαγγειακά νοσήματα και παχυσαρκία, με βάση μελέτες με χαμηλό έως πολύ χαμηλό επίπεδο τεκμηρίωσης.
Συνολικά, η προς το παρόν ακόμη ελλιπής κατάσταση των μελετών δείχνει μια δυσμενή σχέση κινδύνου-οφέλους για την πλειονότητα του πληθυσμού και υποδηλώνει επίσης ότι δεν επιτυγχάνεται στείρα ανοσία (δεν αρρωσταίνει, δεν μολύνει), δηλαδή ότι ο εμβολιασμός δεν είναι κατάλληλος για την προστασία άλλων ατόμων που δεν μπορούν να εμβολιαστούν. Για τους λόγους αυτούς, ο υποχρεωτικός εμβολιασμός δεν είναι ούτε λογικός ούτε δικαιολογημένος. Ο εμβολιασμός μπορεί να γίνεται μόνο σε εθελοντική βάση μετά από ειλικρινή και λεπτομερή ενημέρωση σχετικά με τα οφέλη και τις βλάβες. Η απόφαση για τον εμβολιασμό πρέπει να λαμβάνεται από κοινού από τον γιατρό και τον ασθενή ή τον πολίτη σε μια ενημερωμένη, συμμετοχική διαδικασία λήψης αποφάσεων.
2-Στόχος της παρούσας ανάλυσης
Ο εμβολιασμός κατά της COVID έχει προωθηθεί ως το καλύτερο δυνατό και μοναδικό αποτελεσματικό μέσο για τον τερματισμό της πανδημίας SARS-CoV-2. Ωστόσο, εκτός από το πιο πρόσφατα εγκεκριμένο εμβόλιο με βάση πρωτεΐνες στην Ευρωπαϊκή Ένωση, δεν έχει αναπτυχθεί ή χρησιμοποιηθεί κανένας εμβολιασμός με τη συμβατική μέθοδο. Αντίθετα, με τον “εμβολιασμό” με βάση το mRNA, γενετικά δημιουργημένο, τροποποιημένο mRNA εισάγεται σε ανθρώπινα κύτταρα, όπου μεταφράζεται για να παράγει το πραγματικό ανοσογόνο “πρωτεΐνη εμβολίου” που πρέπει να παραχθεί. Τα “εμβόλια φορέων” έχουν προχωρήσει ένα βήμα παραπέρα και μολύνουν τα ανθρώπινα κύτταρα με έναν γενετικά τροποποιημένο αδενοϊό χιμπατζή, του οποίου το εισαγόμενο γενετικό υλικό στη συνέχεια “επαναπρογραμματίζει” το ανθρώπινο κύτταρο και το αναγκάζει να παράγει την “πρωτεΐνη του εμβολίου”.
Για λόγους απλότητας, αναφερόμαστε ωστόσο σε “εμβολιασμούς” στο παρόν έγγραφο, διότι τόσο τα νανοσωματίδια λιπιδίων που περιέχουν mRNA όσο και οι αδενοϊοί-φορείς χορηγούνται με σκοπό την ανοσοποίηση.
Τους τελευταίους 18 μήνες έχουν χορηγηθεί παγκοσμίως περισσότερα από 11 δισεκατομμύρια εμβόλια COVID, σύμφωνα με το Πανεπιστήμιο Johns Hopkins [1]. Στην Ελλάδα χρησιμοποιήθηκαν περισσότερες από 21 εκατομμύρια δόσεις εμβολίων. Στο 70% περίπου των περιπτώσεων χρησιμοποιήθηκε στην Ελλάδα το εμβόλιο Comirnaty® της BioNTech/Pfizer [2].
Παρά τον μαζικό εμβολιασμό, τον χειμώνα 2021/2022 καταγράφηκε ο υψηλότερος αριθμός νέων μολύνσεων COVID από την αρχή της πανδημίας. Στα τέλη Ιανουαρίου 2022, καταγράφηκαν περίπου 23 εκατομμύρια κρούσματα ανά εβδομάδα παγκοσμίως, αλλά σχετιζόμενα με ένα σημαντικά χαμηλότερο ποσοστό θνησιμότητας των κρουσμάτων, μόλις 0,3% [1]. Ενώ φαίνεται ότι η εξάπλωση της νόσου δεν μπόρεσε να σταματήσει με τους μαζικούς εμβολιασμούς, θεωρείται πιθανό ότι οι επικίνδυνες και θανατηφόρες πορείες νόσου μειώθηκαν με τους εμβολιασμούς. Ωστόσο, η μείωση των σοβαρών κρουσμάτων και των θανάτων θα μπορούσε επίσης να οφείλεται στη μείωση της παθογένειας του ιού ως αποτέλεσμα μεταλλάξεων. Για παράδειγμα, η μετάλλαξη omicron του SARS-CoV-2, η οποία ήρθε πρόσφατα στο προσκήνιο, αποδείχθηκε λιγότερο επικίνδυνη από τις προηγούμενες μεταλλάξεις, ακόμη και στους ανεμβολίαστους [3]. Ταυτόχρονα, αυξάνονται οι αναφορές για ορισμένες σοβαρές παρενέργειες, αλλά και για θανάτους σε σχέση με τον εμβολιασμό COVID [2], ενώ τα δεδομένα από τις ασφαλιστικές εταιρείες υγείας υποδηλώνουν ότι ο αριθμός των παρενεργειών που αναφέρονται στα κυβερνητικά κέντρα μπορεί να είναι πολύ χαμηλότερος από τον πραγματικό αριθμό [4].
Στόχος της παρούσας περίληψης στοιχείων είναι να προσδιοριστούν οι ενδείξεις και οι αντενδείξεις για τον εμβολιασμό με COVID, λαμβάνοντας υπόψη την ηλικία, τις προηγούμενες νόσους, τον κίνδυνο μόλυνσης και τον κίνδυνο παρενεργειών, και να γίνουν σαφείς συστάσεις υπέρ ή κατά του εμβολιασμού για μεμονωμένους ασθενείς. Για το σκοπό αυτό, αναλύονται και παρουσιάζονται η επικινδυνότητα της νόσου και η σχέση κινδύνου-οφέλους του εμβολιασμού με βάση τις διαθέσιμες μελέτες.
Η παρούσα περίληψη δεν αποτελεί συστηματική ανασκόπηση και, ως εκ τούτου, δεν ισχυρίζεται ότι εξαντλεί την επιστημονική βιβλιογραφία. Ωστόσο, έχει ως στόχο να παράσχει μια σαφή συλλογή των σημαντικότερων μελετών και πληροφοριών, ώστε να μπορέσουν οι γιατροί και οι πολίτες να λάβουν μια τεκμηριωμένη, ενημερωμένη και κοινή απόφαση υπέρ ή κατά του εμβολιασμού και να ξεκινήσει ένας εποικοδομητικός επιστημονικός διάλογος μεταξύ των υποστηρικτών και των επικριτών του εμβολιασμού.
Υπό την έννοια μιας “ζωντανής κατευθυντήριας γραμμής”, το παρόν έγγραφο πρέπει να επικαιροποιείται συνεχώς με τα νέα ευρήματα μελετών. Επομένως, η κριτική και οι προτάσεις για αλλαγές και προσθήκες είναι ευπρόσδεκτες.
3-Πόσο επικίνδυνη είναι η COVID;
Στην αρχή της πανδημίας, υπήρχε η υποψία ότι το ποσοστό θνησιμότητας θα ξεπερνούσε το 5% με βάση τα στοιχεία που αναφέρθηκαν από την Κίνα [5]. Ωστόσο, πολύ γρήγορα αποδείχθηκε ότι ο αριθμός αυτός είχε υπερεκτιμηθεί λόγω ελλιπούς καταγραφής των περιπτώσεων. Επομένως, είναι προτιμότερο να μετράται το λεγόμενο ποσοστό θνησιμότητας της λοίμωξης (IFR) μέσω μελετών ορολογικού επιπολασμού σε συνδυασμό με κλινικά δεδομένα, προκειμένου να εκτιμηθεί ο κίνδυνος μιας μεταδοτικής νόσου. Το ποσοστό αυτό ήταν 0,36% σε μια πρώιμη γερμανική μελέτη [6] και μόνο 0,15% σε μια μεγάλη διεθνή μετα-ανάλυση [7]. Η IFR του COVID είναι επομένως ασήμαντα υψηλότερη από την υποτιθέμενη μέση IFR της γρίπης του 0,12% (υπολογισμένη από δεδομένα του CDC από το 2010-2020) [8].
Επιπλέον, διαπιστώθηκε έντονη εξάρτηση της IFR από την ηλικία. Σύμφωνα με μια μετα-ανάλυση 27 μελετών που αξιολόγησαν το IFR σε ηλικιακή βάση, το ποσοστό αυτό κυμαινόταν μεταξύ 0,002% για τους 10χρονους και 15-20% για τους άνω των 85 ετών. Αυτό σημαίνει ότι η COVID είναι περίπου 7.500-10.000 φορές πιο επικίνδυνη για τους πολύ ηλικιωμένους απ’ ό,τι για τα παιδιά. Η σχέση είναι λογαριθμογραμμική. Σχετική αύξηση της επικινδυνότητας παρατηρείται μόνο από την ηλικία των 50 ετών περίπου. Περίπου σε αυτή την ηλικία, το IFR της COVID υπερβαίνει το μέσο IFR της γρίπης(0,12%).
Εκτός από την ηλικία, ωστόσο, σημαντικό ρόλο παίζει και η προϋπάρχουσα και συνοδός νοσηρότητα. Σε μια ιταλική μελέτη που διεξήχθη κατά τη διάρκεια του πρώτου καταστροφικού κύματος COVID στη Λομβαρδία, αποδείχθηκε ότι το 99,2% των ατόμων που πέθαναν από ή με COVID είχαν τουλάχιστον μία συννοσηρότητα [9]. Το 25% είχε μία ή δύο συννοσηρότητες και σχεδόν το 50% είχε τρεις ή περισσότερες. Οι πιο συχνές συννοσηρότητες ήταν η ισχαιμική καρδιοπάθεια, ο σακχαρώδης διαβήτης, ο καρκίνος και η κολπική μαρμαρυγή.
Κατά την αξιολόγηση των ενδείξεων, των αντενδείξεων και της σχέσης κινδύνου-οφέλους των εμβολιασμών COVID, ο κίνδυνος σοβαρής ή θανατηφόρας εξέλιξης της νόσου πρέπει να συνυπολογίζεται σε κάθε μεμονωμένη περίπτωση, προκειμένου να ληφθεί μια ισορροπημένη, τεκμηριωμένη απόφαση.
Σύμφωνα με μια πρώιμη κινεζική μελέτη, η COVID του τύπου Wuhan εξελίσσεται στο >80% των συμπτωματικών περιπτώσεων ως μια κοινότυπη γριπώδης λοίμωξη, στην καλύτερη περίπτωση παρόμοια με ένα κρυολόγημα, στην πιο έντονη περίπτωση παρόμοια με μια μη επιπλεγμένη γρίπη. Περίπου το 15% είχε πιο σοβαρή πορεία της ασθένειας. Στο 5% των περιπτώσεων, η νόσος έγινε κρίσιμη και χρειάστηκε εντατική φροντίδα [10]. Όπως η CFR και η IFR, η κατανομή των ήπιων, σοβαρών και πιο σοβαρών περιπτώσεων εξαρτάται φυσικά από την ηλικία και τη συννοσηρότητα του πληθυσμού που μελετάται. Οι μεταλλάξεις μείωσαν το ποσοστό των σοβαρών νόσων. Έτσι, για την παραλλαγή Omikron, αναφέρεται ποσοστό νοσηλείας (ως ένδειξη σοβαρής νόσου) μόλις 2,5% [11].
Σύμφωνα με μια συστηματική ανασκόπηση με μετα-ανάλυση, περίπου το 30% όλων των λοιμώξεων με SARS-CoV-2 είναι εντελώς ασυμπτωματικές [12]. Με την παραλλαγή omicron, το ποσοστό αυτό θα μπορούσε να είναι σημαντικά υψηλότερο, αλλά δεν υπάρχουν επί του παρόντος αξιόπιστες επιστημονικές δημοσιεύσεις σχετικά με αυτό. Δεν είναι επίσης σαφές αν αυτό είναι συνέπεια της μειωμένης ιογένεσης του μεταλλαγμένου ιού ή αποτέλεσμα του εμβολιασμού.
Συμπέρασμα: Συνοψίζοντας, μπορεί να δηλωθεί ότι ο παγκόσμιος μέσος κίνδυνος COVID είναι στο εύρος της εποχικής γρίπης ή ασήμαντα υψηλότερος. Σύμφωνα με τις τρέχουσες γνώσεις, ο κίνδυνος της παραλλαγής omicron είναι σίγουρα μικρότερος από τον κίνδυνο της γρίπης. Ωστόσο, υπάρχει ισχυρή εξάρτηση από την ηλικία και την παρουσία συννοσηρότητας. Οι νέοι και υγιείς, αλλά και οι ηλικιωμένοι υγιείς άνθρωποι έχουν πολύ χαμηλό κίνδυνο σοβαρής ή ακόμη και θανατηφόρας εξέλιξης της COVID. Αυτό πρέπει να λαμβάνεται υπόψη όταν εξετάζεται η σχέση κινδύνου-οφέλους ενός εμβολιασμού κατά της COVID-19.
4-Προστασία του εμβολιασμού από συμπτωματική λοίμωξη, σοβαρή πορεία και θάνατο
4.1-Προστασία μέσω της βασικής ανοσοποίησης κατά της συμπτωματικής λοίμωξης
Οι μελέτες έγκρισης των τεσσάρων πρώτων εμβολίων COVID που εγκρίθηκαν με διαδικασίες fast-track στην Ευρωπαϊκή Ένωση τον Δεκέμβριο του 2020 (τα mRNA εμβόλια Comirnaty® και Spikevax® και τα εμβόλια-φορείς Vaxzevria® και Jcovden®) δείχνουν υψηλή προστατευτική αποτελεσματικότητα έναντι συμπτωματικών λοιμώξεων που προκαλούνται από τον SARS-CoV-2 στις δημοσιεύσεις του ειδικού τύπου [13-16], όπως και το αδρανοποιημένο εμβόλιο Nuvaxovid® [17,18], το οποίο έλαβε έκτακτη έγκριση μόλις τον Δεκέμβριο του 2021 (βλ. Πίνακα 1).
| Εμπορική ονομασία | Γενική ονομασία | Κατασκευαστής | Αποτελεσματικότητα του εμβολίου όσον αφορά τη συμπτωματική λοίμωξη (%) |
| Comirnaty® | BNT162b2 | Pfizer/BioNTech | 95,0 |
| Spikevax® | mRNA-1273 | Moderna | 94,1 |
| Vaxzevria® | AZD1222 | AstraZeneca | 62,1 |
| Jcovden® | Ad26.COV2.S | Jansen | 66,9 |
| Nuvaxovid® | NVX-CoV2373 | Novavax | 89,7 |
Ωστόσο, σε όλες τις μελέτες καταγραφής, η μέτρηση της αποτελεσματικότητας του εμβολίου δεν αρχίζει πριν από επτά ημέρες μετά τον τελευταίο εμβολιασμό. Ωστόσο, δεδομένου ότι στην πραγματικότητα δεν είναι δυνατόν να “παραλειφθεί” η ευάλωτη περίοδος μεταξύ του πρώτου εμβολιασμού και της ανάπτυξης πλήρους εμβολιαστικής προστασίας από τη δεύτερη εβδομάδα μετά τον τελευταίο εμβολιασμό, τα αποτελέσματα όλων των μελετών καταγραφής πρέπει να επικριθούν από μεθοδολογική άποψη και ισχύουν μόνο σε περιορισμένο βαθμό. Επιπλέον, αξιολογούνται μόνο οι λοιμώξεις που είναι θετικές στη δοκιμή PCR και όχι όλες οι συμπτωματικές ύποπτες περιπτώσεις COVID-19. Έτσι, δεν λαμβάνεται υπόψη η χαμηλή ευαισθησία της εξέτασης PCR και η πιθανώς αυξημένη ευαισθησία των εμβολιασμένων ατόμων σε άλλες αναπνευστικές νόσους.
Τα έγγραφα έγκρισης που υποβλήθηκαν στον FDA για το Comirnaty® δίνουν επίσης τα στοιχεία για τα ύποπτα κρούσματα που δεν επιβεβαιώθηκαν με τη δοκιμή PCR. Από αυτά, 1.594 συνέβησαν στην ομάδα των εμβολιασμένων και 1.816 στην ομάδα του εικονικού φαρμάκου, γεγονός που αντιστοιχεί σε αποτελεσματικότητα του εμβολίου μόλις 12,2%. Τις πρώτες επτά ημέρες μετά τον εμβολιασμό, υπήρχαν σημαντικά περισσότερα ύποπτα κρούσματα μεταξύ των εμβολιασμένων, με 409 κρούσματα στην ομάδα εμβολιασμού και μόνο 287 στην ομάδα εικονικού φαρμάκου (RR 1,44, 95% CI 1,24-1,67, που αντιστοιχεί σε αύξηση του κινδύνου κατά 44% λόγω του εμβολιασμού) [19].
Επιπλέον, πρέπει να επικριθεί η σύντομη περίοδος παρατήρησης όλων των μελετών καταγραφής, η οποία δεν επιτρέπει μια δήλωση σχετικά με τη διάρκεια της προστασίας από τον εμβολιασμό. Όσον αφορά τη μέτρηση της αποτελεσματικότητας, η περίοδος παρατήρησης ήταν μόνο 6-8 εβδομάδες, ενώ όσον αφορά την ασφάλεια, μόνο 12-14 εβδομάδες. Τα πρωτόκολλα μελέτης και οι καταχωρίσεις μελετών καθιστούν σαφές ότι όλες οι μελέτες καταχώρισης έχουν σχεδιαστεί για προγραμματισμένη περίοδο παρατήρησης 26 μηνών. Συνεπώς, τα δημοσιευμένα αποτελέσματα πρέπει να αξιολογούνται στην καλύτερη περίπτωση ως πρώιμα ενδιάμεσα αποτελέσματα [20].
Επίσης, θα πρέπει να σημειωθεί για τις δύο μελέτες mRNA ότι οι μελέτες καταχώρισης δεν είναι διπλές-τυφλές μελέτες. Ωστόσο, αυτό δεν προκύπτει σαφώς από τις δημοσιεύσεις στο New England Journal of Medicine. Η δημοσίευση κάνει λόγο για “τυφλή από τον παρατηρητή” και παραμένει ανοιχτό τι εννοείται με αυτό. Ωστόσο, αυτό αναφέρεται ρητά στα πρωτόκολλα μελετών των εταιρειών: Μόνο οι συμμετέχοντες και το προσωπικό της μελέτης που πραγματοποίησε την αξιολόγηση ήταν «τυφλοί», αλλά όχι το ιατρικό προσωπικό που πραγματοποίησε τις ενέσεις του εμβολίου ή του εικονικού φαρμάκου [20,21]. Λόγω των πολύ συχνών τοπικών αντιδράσεων του εμβολιασμού, οι οποίες εμφανίστηκαν πολύ σπάνια μετά το εικονικό φάρμακο, πρέπει επίσης να υποτεθεί ότι τα περισσότερα άτομα μπορούσαν τουλάχιστον να μαντέψουν αν τους χορηγήθηκε εικονικό φάρμακο ή εμβόλιο. Η έλλειψη τυφλότητας ενέχει υψηλό κίνδυνο μεροληψίας.
Τέλος, σε αντίθεση με τις αρχές της ιατρικής που βασίζεται σε αποδείξεις, στις μελέτες καταχώρισης επιλέχθηκε ένα κλινικά μόνο οριακά σχετικό πρωτεύον καταληκτικό σημείο. Η συμπτωματική λοίμωξη COVID, μια κοινότυπη λοίμωξη που μοιάζει με γρίπη, είναι εντελώς ασήμαντη για τους περισσότερους ανθρώπους και ο εμβολιασμός κατά αυτής είναι συνεπώς άκυρος. Από τις μελέτες καταγραφής δεν μπορούν να εξαχθούν αξιόπιστες δηλώσεις σχετικά με την αποτελεσματικότητα του εμβολιασμού όσον αφορά τα πραγματικά σημαντικά τελικά σημεία, δηλαδή την πρόληψη σοβαρών ασθενειών και θανάτων, επειδή τα περιστατικά είναι πολύ λίγα.
Μόνο για το Comirnaty® δημοσιεύθηκε μια περαιτέρω ενδιάμεση αξιολόγηση μετά από έξι μήνες παρακολούθησης [22]. Ωστόσο, ο πραγματικός μέσος χρόνος παρατήρησης των συμμετεχόντων στη μελέτη σε αυτή την περαιτέρω ενδιάμεση αξιολόγηση ήταν επίσης μόνο λίγο πάνω από τέσσερις μήνες. Εντός αυτής της περιόδου παρατήρησης, μόνο ένα εμβολιασμένο άτομο εμφάνισε σοβαρή νόσο COVID, ενώ στην ομάδα του εικονικού φαρμάκου καταγράφηκαν 30 σοβαρά περιστατικά. Αυτό αντιστοιχεί σε αποτελεσματικότητα εμβολιασμού 96,7%. Ωστόσο, ακόμη και σε αυτή την παρατήρηση, λήφθηκαν υπόψη μόνο οι περιπτώσεις θετικών στο test PCR που συνέβησαν τουλάχιστον επτά ημέρες μετά τον τελευταίο εμβολιασμό και το χαμηλό ποσοστό συμβάντων καθιστά το συνολικό αποτέλεσμα αβέβαιο. Το συνολικό ποσοστό νοσηλείας δεν αναφέρεται.
Ωστόσο, η εν λόγω δημοσίευση αναφέρει τουλάχιστον τη συνολική θνησιμότητα στους ασθενείς που εμβολιάστηκαν με Comirnaty® σε σύγκριση με τους ασθενείς που έλαβαν εικονικό φάρμακο: 15 θάνατοι σημειώθηκαν στην ομάδα που εμβολιάστηκε και 14 στην ομάδα που έλαβε εικονικό φάρμακο [22]. Ο κίνδυνος θανάτου ήταν επομένως περίπου ο ίδιος και στις δύο ομάδες. Οι αριθμοί δίνονται μόνο στο ηλεκτρονικό παράρτημα. Λόγω του χαμηλού αριθμού συμβάντων, δεν είναι δυνατή μια αξιόπιστη δήλωση σχετικά με την αποτελεσματικότητα του εμβολιασμού όσον αφορά το θάνατο και τη νοσηλεία από τις μεμονωμένες μελέτες καταγραφής.
Σε μια μετα-ανάλυση (προδημοσίευση ακόμη χωρίς αξιολόγηση από ομοτίμους), εξετάστηκε και συνοψίστηκε η συνολική θνησιμότητα σε όλες τις διαθέσιμες τυχαιοποιημένες ελεγχόμενες δοκιμές των εμβολίων mRNA και των εμβολίων-φορέων. Δεν βρέθηκε καμία επίδραση στην ολική θνησιμότητα για τα εμβόλια mRNA (σχετικός κίνδυνος 1,03, 95% CI 0,63-1,71), αλλά υπήρξε επίδραση για τα εμβόλια φορέων (σχετικός κίνδυνος 0,37, 95% CI 0,19-0,70). Οι συγγραφείς αποδίδουν το πλεονέκτημα των εμβολίων φορέων σε μη ειδικές ανοσολογικές επιδράσεις. Ωστόσο, δεδομένου του μικρού αριθμού περιπτώσεων και των σύντομων περιόδων παρατήρησης, το αποτέλεσμα θα μπορούσε να είναι απλώς τυχαίο. Στο συμπέρασμά τους, οι συγγραφείς ζητούν, επομένως, ορθά να διεξαχθούν περαιτέρω τυχαιοποιημένες ελεγχόμενες συγκριτικές μελέτες με μεγαλύτερες περιόδους παρατήρησης [23].
Συμπέρασμα: Κατά τις πρώτες εβδομάδες μετά την ολοκλήρωση των εμβολιασμών, προκύπτει υψηλή αποτελεσματικότητα του εμβολιασμού όσον αφορά την πρόληψη συμπτωματικών λοιμώξεων από COVID με θετικό τεστ PCR. Η αποτελεσματικότητα είναι σημαντικά χαμηλότερη όταν λαμβάνεται υπόψη ο ευάλωτος χρόνος μεταξύ του πρώτου εμβολιασμού και της πλήρους ανάπτυξης της προστασίας. Δεν έχει ακόμη αποδειχθεί η επίδραση του εμβολιασμού στην ολική θνησιμότητα. Συμπεράσματα σχετικά με τη μακροπρόθεσμη αποτελεσματικότητα των εμβολίων δεν μπορούν να εξαχθούν λόγω των πολύ μικρών περιόδων παρατήρησης. Η ελλιπής τυφλότητα στις μελέτες mRNA θα μπορούσε επίσης να είναι η αιτία της μεροληψίας στα αποτελέσματα της μελέτης.
4.2-Αποτελεσματικότητα του εμβολίου της βασικής ανοσοποίησης σε αναδρομικές μελέτες παρατήρησης όσον αφορά τη σοβαρή νόσο και το θάνατο
Όπως περιγράφηκε στην τελευταία ενότητα, από τις μελέτες καταγραφής δεν μπορούν να εξαχθούν αξιόπιστες δηλώσεις σχετικά με την αποτελεσματικότητα του εμβολίου όσον αφορά τις σοβαρές πορείες και το θάνατο. Εν τω μεταξύ, έχουν δημοσιευθεί διάφορες αναδρομικές μελέτες παρατήρησης για το θέμα αυτό.
Ένα σημαντικό παράδειγμα τέτοιας μελέτης είναι μια μεγάλη μελέτη αντιστοιχισμένης κοορτής από το Ισραήλ, στην οποία 596.618 άτομα εμβολιασμένα με Comirnaty® και μη εμβολιασμένα συγκρίθηκαν ως προς τον κίνδυνο νοσηλείας ή θανάτου που σχετίζεται με την COVID [24]. Η σχετική μείωση του κινδύνου των εμβολιασμένων ατόμων όσον αφορά τη νοσηλεία αναφέρεται ότι είναι 74% στις 14 ημέρες μετά τον πρώτο εμβολιασμό (CI 56-86%), αλλά όταν αναλύονται οι ακατέργαστοι αριθμοί, στην πραγματικότητα ήταν μόνο 58% (110 εμβολιασμένοι νοσηλευόμενοι, 259 μη εμβολιασμένοι νοσηλευόμενοι) – που είναι ήδη πολύ μικρότερη από ό,τι πρότειναν οι μελέτες καταγραφής. Η απόλυτη μείωση του κινδύνου, η οποία δεν αναφέρεται στη δημοσίευση αλλά μπορεί να υπολογιστεί από τα δημοσιευμένα στοιχεία, ήταν μόλις 0,025%. Αυτό σημαίνει ότι περίπου 4.000 άτομα πρέπει να εμβολιαστούν για να αποφευχθεί μια νοσηλεία που σχετίζεται με την COVID. Όσον αφορά την πρόληψη ενός θανάτου που σχετίζεται με COVID, ο απόλυτος κίνδυνος μειώνεται μόνο κατά 0,0039% μέσω του εμβολιασμού. Αυτό σημαίνει ότι περίπου 26.000 άτομα πρέπει να εμβολιαστούν για να αποφευχθεί ένας θάνατος που σχετίζεται με την COVID. Επομένως, η πιθανότητα να προστατευθεί το άτομο από τον εμβολιασμό είναι εξαιρετικά χαμηλή και πρέπει συνεπώς να σταθμιστεί έναντι των κινδύνων του εμβολιασμού.
Ένα σημαντικό πρόβλημα της μελέτης αυτής είναι ότι αξιολογήθηκαν μόνο τα συμβάντα που συνέβησαν τουλάχιστον 14 ημέρες μετά τον πρώτο εμβολιασμό ή ακόμη περισσότερο από 7 ημέρες μετά τον δεύτερο εμβολιασμό. Αυτό σημαίνει ότι, για παράδειγμα, οι νοσηλείες και οι θάνατοι που οφείλονται στον εμβολιασμό κατά τις πρώτες 14 ημέρες μετά τον εμβολιασμό δεν αξιολογήθηκαν και δεν αναφέρθηκαν καθόλου.
Ένα άλλο σημείο είναι ότι αναφέρθηκαν μόνο οι ειδικές για την COVID νοσηλείες και θάνατοι και όχι το συνολικό ποσοστό νοσηλείας και η συνολική θνησιμότητα.
Επιπλέον, πρέπει να επικριθεί το γεγονός ότι αποκλείστηκαν από τη συμμετοχή στη μελέτη όλα τα άτομα που εργάζονται στον τομέα της υγείας, οι κάτοικοι οίκων ευγηρίας, τα άτομα που χρειάζονται φροντίδα και ζουν στο σπίτι τους, τα άτομα που είχαν επαφή με το σύστημα υγείας τις τρεις προηγούμενες ημέρες και εκείνοι που είχαν νοσήσει με COVID. Συνεπώς, δεν μπορούν να εξαχθούν από τη μελέτη συμπεράσματα ακριβώς για τα άτομα που πιθανότατα θα ωφεληθούν από τον εμβολιασμό.
Τέλος, πρέπει επίσης να ληφθεί υπόψη ότι ο μέσος χρόνος παρατήρησης για τον κάθε συμμετέχοντα στην παρούσα μελέτη ήταν μόλις 15 ημέρες. Ως εκ τούτου, είναι δύσκολο να εξαχθούν συμπεράσματα σχετικά με τη μακροπρόθεσμη αποτελεσματικότητα του εμβολιασμού.
Εν τω μεταξύ, είναι διαθέσιμες πολυάριθμες άλλες μελέτες παρατήρησης με παρόμοια αποτελέσματα, στις οποίες ισχύουν σε γενικές γραμμές τα ίδια σημεία που κατακρίνουμε, ιδίως η μη συνεκτίμηση των συμβάντων κατά τις πρώτες εβδομάδες μετά τον εμβολιασμό και η έλλειψη αναφοράς για τα συνολικά ποσοστά νοσηλείας και την ολική θνησιμότητα [25-27].
Συμπέρασμα: Λαμβάνοντας υπόψη μόνο τα ειδικά για την COVID καταληκτικά σημεία και εξαιρώντας την ευάλωτη περίοδο μεταξύ του πρώτου εμβολιασμού και της ανάπτυξης εμβολιαστικής προστασίας, υπάρχει σαφής αποτελεσματικότητα του εμβολίου στην πρόληψη της νοσηλείας και του θανάτου λόγω COVID, αλλά αυτή περιορίζεται σε μια πολύ σύντομη περίοδο παρατήρησης 15 ημερών. Ωστόσο, δεν υπάρχουν ισχυρά στοιχεία από μελέτες που να υποστηρίζουν τη μείωση της συνολικής νοσηλείας και της συνολικής θνησιμότητας και παραμένει ασαφές πόσο διαρκεί η μετρούμενη προστασία από το εμβόλιο.
4.3-Αποτελεσματικότητα των αναμνηστικών εμβολιασμών
Η μελέτη των Barda et al [28] αναφέρεται κυρίως ως απόδειξη για την αποτελεσματικότητα του αναμνηστικού εμβολιασμού στην πρόληψη της σοβαρής εξέλιξης της νόσου και των θανάτων που σχετίζονται με την COVID. Στη μελέτη αυτή, 738.321 άτομα με αναμνηστικό εμβολιασμό συγκρίθηκαν με τον ίδιο αριθμό ατόμων που εμβολιάστηκαν διπλά χωρίς αναμνηστικό εμβολιασμό. Για τα άτομα που εμβολιάστηκαν με αναμνηστικό εμβολιασμό, η περίοδος παρατήρησης ξεκίνησε μόλις επτά ημέρες μετά τον αναμνηστικό εμβολιασμό. Ο μέσος (διάμεσος) χρόνος παρατήρησης ήταν μόλις 13 ημέρες. Το αποτέλεσμα ήταν ότι, μόνο η νοσηλεία “σχετιζόμενη με COVID”, η σοβαρή ασθένεια “σχετιζόμενη με COVID” και ο θάνατος “σχετιζόμενος με COVID” βαθμολογήθηκαν από την 8η ημέρα μετά τον εμβολιασμό. Ο συνολικός αριθμός των νοσηλειών, των σοβαρών άλλων ασθενειών και των θανάτων δεν αναφέρεται, ιδίως κατά τις πρώτες επτά ημέρες μετά τον εμβολιασμό. Εξαιρέθηκαν τα άτομα που εργάζονταν σε εγκαταστάσεις φροντίδας και όσοι εργάζονταν στον τομέα της υγείας. Στην ομάδα που εμβολιάστηκε μόνο δύο φορές, υπήρξαν 231 νοσηλείες που σχετίζονταν με COVID (0,03%), 157 σοβαρές ασθένειες COVID (0,02%) και 44 νοσηλείες που σχετίζονταν με θανάτους COVID (0,006%). Στους ασθενείς που έλαβαν τη booster, παρατηρήθηκαν μόνο 29 νοσηλείες που σχετίζονταν με COVID (0,004%), 17 σοβαρές νοσήσεις (0,002%) και 7 θάνατοι (0,001%). Οι απόλυτες μειώσεις του κινδύνου, οι οποίες επίσης δεν αναφέρθηκαν στη δημοσίευση της μελέτης, αλλά μπορούν να υπολογιστούν από τα στοιχεία που παρουσιάζονται, ήταν 0,026%, 0,018% και 0,005%.
Καμία δήλωση δεν μπορούσε να γίνει για την ηλικιακή ομάδα κάτω των 40 ετών λόγω ελλειπόντων συμβάντων, και ο πληθυσμός με τον υψηλότερο κίνδυνο για σοβαρή πορεία COVID (κάτοικοι οίκων ευγηρίας) είχε ήδη αποκλειστεί από το σχεδιασμό.
Τα απόλυτα αποτελέσματα είναι επομένως οριακά. Επιπλέον, η μελέτη έχει σημαντικές μεθοδολογικές αδυναμίες, τις οποίες οι συγγραφείς της μελέτης συζητούν επίσης ανοιχτά. Πάνω απ’ όλα, θα πρέπει να επισημανθούν τα γενικά προβλήματα των αναδρομικών μελετών παρατήρησης (μη ανιχνεύσιμη σύγχυση, παράδοξο του Simpson, μεροληψία επιλογής κ.λπ.). Φυσικά, μια περίοδος παρατήρησης 13 ημερών κατά μέσο όρο δεν μπορεί να χρησιμοποιηθεί για την εξαγωγή συμπερασμάτων σχετικά με τη μακροπρόθεσμη αποτελεσματικότητα του αναμνηστικού εμβολιασμού. Η έλλειψη συνολικής θνησιμότητας και συνολικών ποσοστών νοσηλείας και το γεγονός ότι η περίοδος παρατήρησης άρχισε μόνο επτά ημέρες μετά τον αναμνηστικό εμβολιασμό (δηλαδή εξαιρείται η περίοδος με τον υψηλότερο κίνδυνο για παρενέργειες) μειώνουν σημαντικά την αξία της μελέτης.
Η μελέτη των Bar-On et al. θεωρείται ως περαιτέρω απόδειξη για την αποτελεσματικότητα του αναμνηστικού εμβολιασμού [29]. Στην εν λόγω μελέτη, συνολικά περίπου 1,1 εκατομμύρια ασφαλισμένοι άνω των 60 ετών παρακολουθήθηκαν κατά μέσο όρο για περίπου 10 ημέρες. Ο αναμνηστικός εμβολιασμός έπρεπε να έχει πραγματοποιηθεί τουλάχιστον 12 ημέρες πριν. Στην προσαρμοσμένη ανάλυση, ο κίνδυνος λοίμωξης από COVID ήταν 11,3 φορές υψηλότερος για όσους είχαν εμβολιαστεί δύο φορές από ό,τι για όσους είχαν λάβει την ενισχυτική δόση, και ο κίνδυνος σοβαρής εξέλιξης της νόσου ήταν 19,5 φορές υψηλότερος. Ωστόσο, τα απόλυτα αποτελέσματα ήταν επίσης οριακά σε αυτή τη μελέτη. Δεν αναφέρονται συνολικά ποσοστά νοσηλείας και θνησιμότητας. Συνεπώς, η μελέτη δεν επιτρέπει μια εξαγωγή συμπεράσματος σχετικά με το συνολικό ποσοστό νοσηλείας και θνησιμότητας, συμπεριλαμβανομένου του χρόνου αμέσως μετά τον εμβολιασμό, ούτε σχετικά με την αποτελεσματικότητα του αναμνηστικού εμβολίου σε νέους, υγιείς ανθρώπους, ούτε σχετικά με τις μακροπρόθεσμες επιπτώσεις μετά το αναμνηστικό εμβόλιο.
Μέχρι σήμερα, υπάρχει μόνο μία αναδρομική μελέτη κοόρτης που εξετάζει τη συνολική θνησιμότητα σε σύγκριση μεταξύ των ανεμβολίαστων, των απλά εμβολιασμένων, των διπλά εμβολιασμένων και των ενισχυμένων [30]. Σε μια πολυπαραγοντική ανάλυση, η μελέτη αυτή καταλήγει στο συμπέρασμα ότι οι ανεμβολίαστοι έχουν τριπλάσιο κίνδυνο θνησιμότητας από τους ενισχυμένους. Ωστόσο, οι απλά εμβολιασμένοι πεθαίνουν δύο φορές συχνότερα από τους ανεμβολίαστους και οι διπλά εμβολιασμένοι, των οποίων ο τελευταίος εμβολιασμός έγινε πριν από έξι μήνες, ακόμη και τέσσερις φορές συχνότερα. Η μελέτη έχει περίοδο παρατήρησης μόνο τριών μηνών και όλοι οι αναμνηστικοί εμβολιασμοί εμπίπτουν σε αυτή την περίοδο παρατήρησης, οπότε η πραγματική περίοδος παρατήρησης για τους αναμνηστικούς είναι πολύ μικρότερη από ό,τι για τους ανεμβολίαστους. Όλα τα μη εμβολιασμένα άτομα που εμβολιάστηκαν κατά τη διάρκεια της περιόδου μελέτης υπολογίζονται ως εμβολιασμένα στην αξιολόγηση. Επομένως, θα έπρεπε να βασιστούν οι θάνατοι όχι μόνο στην κατάσταση εμβολιασμού, αλλά και στους ανθρωπομήνες κινδύνου. Ο αποκλεισμός των ενοίκων οίκων ευγηρίας και των ατόμων που προσβλήθηκαν από COVID κατά τη διάρκεια της περιόδου μελέτης αυξάνει την πιθανή μεροληψία επιλογής [30]. Συνεπώς, η μελέτη είναι ελάχιστα κατάλληλη για την απόδειξη της αποτελεσματικότητας όσον αφορά την ολική θνησιμότητα.
Συμπέρασμα: Ο αναμνηστικός εμβολιασμός περίπου έξι μήνες μετά την ολοκλήρωση του βασικού εμβολιασμού οδηγεί ενδεχομένως σε μείωση της σοβαρής εξέλιξης της COVID και των θανάτων που σχετίζονται με COVID σε άτομα ηλικίας άνω των 60 ετών. Ωστόσο, η δήλωση αυτή αποδυναμώνεται από σοβαρά μεθοδολογικά σφάλματα στις μελέτες. Δεν έχει ακόμη αποδειχθεί επίδραση στο ποσοστό νοσηλείας και θανάτου από COVID σε νεαρά, υγιή άτομα. Από τις διαθέσιμες μελέτες δεν μπορούν να εξαχθούν δηλώσεις σχετικά με το συνολικό ποσοστό νοσηλείας και τη συνολική θνησιμότητα.
4.4-Διάρκεια της προστασίας από τους εμβολιασμούς COVID
Όπως φαίνεται ήδη από τις παρουσιάσεις των τυχαιοποιημένων ελεγχόμενων μελετών καταγραφής και των αναδρομικών μελετών παρατήρησης, δεν μπορεί να εξαχθεί ασφαλές συμπέρασμα σχετικά με τη διάρκεια της προστασίας από τον εμβολιασμό κατά της COVID σε καμία από αυτές τις μελέτες, καθώς οι περίοδοι παρατήρησης ήταν πολύ σύντομες για κάτι τέτοιο.
Εν τω μεταξύ, υπάρχουν πολυάριθμες ενδείξεις ότι η αποτελεσματικότητα όσον αφορά την πρόληψη μιας λοίμωξης ή μιας σοβαρής εξέλιξης μειώνεται σαφώς μέσα σε λίγους μήνες. Η πρώτη ένδειξη εντοπίζεται ήδη στην εξάμηνη παρακολούθηση της δοκιμής καταχώρισης για το BNT162b2 (Comirnaty®) με μέσο χρόνο παρακολούθησης περίπου 4 μήνες μετά τον πρώτο εμβολιασμό. Σε σύγκριση με την αξιολόγηση των πρώτων 6-8 εβδομάδων [13] με αποτελεσματικότητα του εμβολιασμού 95%, αυτή μειώνεται ήδη στο 84% μετά από τέσσερις μήνες [22].
Σε μια σουηδική μελέτη, η αποτελεσματικότητα του εμβολίου στην πρόληψη της λοίμωξης SARS-CoV-2 οποιασδήποτε σοβαρότητας αποδείχθηκε ότι ήταν 92% 15-30 ημέρες μετά τον δεύτερο εμβολιασμό, μειώθηκε σε 23% και έχασε τη βαρύτητά της μετά από περίπου 200 ημέρες (95% CI -2 έως 41%) [31].
Μια ισραηλινή μελέτη παρατήρησης έδειξε επίσης ότι τόσο ο γενικός κίνδυνος μόλυνσης όσο και ο κίνδυνος σοβαρής εξέλιξης της COVID είναι σχεδόν διπλάσιος σε άτομα των οποίων ο τελευταίος εμβολιασμός έγινε πριν από έξι μήνες σε σχέση με εκείνους που εμβολιάστηκαν πριν από τέσσερις μήνες [32].
Μια αμερικανική αναδρομική μελέτη κοόρτης έδειξε ότι η αποτελεσματικότητα του εμβολίου BNT162b2 όσον αφορά τη μόλυνση μειώθηκε από 88% σε 47% εντός πέντε μηνών [33].
Όλες αυτές οι μελέτες βασίζονται επίσης στις μεθοδολογικές ατέλειες ότι οι λοιμώξεις αξιολογούνται μόνο από μια ορισμένη περίοδο μετά τον τελευταίο εμβολιασμό και ότι δεν παρουσιάζονται στοιχεία σχετικά με το συνολικό ποσοστό νοσηλείας και τη συνολική θνησιμότητα.
Συμπέρασμα: Όπως είναι γνωστό για τα ιογενή κρυολογήματα, η μόλυνση από ιούς του κρυολογήματος δεν δημιουργεί μόνιμη ανοσολογική προστασία. Το ίδιο ισχύει προφανώς και για τους εμβολιασμούς κατά της COVID, όπως είναι επίσης γνωστό από τον εμβολιασμό κατά της γρίπης. Οποιαδήποτε προστασία μπορεί να υπάρχει τις πρώτες εβδομάδες μετά τον πλήρη εμβολιασμό χάνεται και πάλι μέσα σε λίγους μήνες. Επομένως, η μόνιμη εξάλειψη του SARS-CoV2 μέσω εμβολιασμού είναι εξίσου μικρή όσο και η ανάπτυξη αποτελεσματικής ανοσίας αγέλης.
4.5-Αποτελεσματικότητα των διαθέσιμων εμβολίων κατά των μεταλλάξεων του SARS-CoV-2
Όλα τα εμβόλια που διατίθενται στην Ευρώπη στρέφονται κατά αντιγόνων του αρχικού τύπου Wuhan του SARS-CoV-2. Όπως είναι χαρακτηριστικό για τους ιούς RNA, συχνές μεταλλάξεις συμβαίνουν και στον SARS-CoV-2 και έτσι σχηματίζονται νέες παραλλαγές του ιού [34]. Από την πρώτη πανδημική εξάπλωση του ιού, έχουν εντοπιστεί πολυάριθμες μεταλλάξεις του ιού, οι περισσότερες από τις οποίες δεν διαδραματίζουν σημαντικό επιδημιολογικό ρόλο και ταξινομούνται ως “παραλλαγές ενδιαφέροντος”, παραλλαγές υπό παρακολούθηση” ή “παραλλαγές αποκλιμάκωσης”. Μόνο λίγες παραλλαγές θεωρούνται “παραλλαγές που προκαλούν ανησυχία”, καθώς είναι είτε πιο μολυσματικές από τις προηγούμενες μεταλλάξεις ή σχετίζονται με πιο σοβαρή εξέλιξη της νόσου. Μέχρι στιγμής, μόνο οι μεταλλάξεις άλφα (B1.1.7), βήτα (B.1.351), γάμμα (P.1), δέλτα (B.1.617.2) και όμικρον (B.1.1.529-BA.1 και BA.2, πιο πρόσφατα επίσης BA.4 και BA.5, οι οποίες προκαλούν “καλοκαιρινό κύμα” από τον Ιούνιο του 2022) έχουν σημαντική επιδημιολογική σημασία [35].
Για τον έλεγχο της πανδημίας, το σημαντικό ερώτημα είναι αν τα εμβόλια που απευθύνονται στα αντιγόνα του πρωτότυπου ιού προστατεύουν επίσης από τη νόσο και τη μόλυνση από μεταλλάξεις.
Μια συστηματική ανασκόπηση της αποτελεσματικότητας του εμβολίου έναντι των μεταλλάξεων άλφα, βήτα και γάμμα, η οποία περιελάμβανε 35 μελέτες, έδειξε μόνο ελαφρώς μειωμένη αποτελεσματικότητα μεταξύ 70% και 100% (21 μελέτες) για την μετάλλαξη άλφα σε σύγκριση με τις μελέτες καταγραφής, αντιφατικά αποτελέσματα για την μετάλλαξη βήτα (αποτελεσματικότητα του εμβολίου μεταξύ 21,9% και 100%, επτά μελέτες) και σημαντικά μειωμένη αποτελεσματικότητα 36,8% και 46,8% (δύο μελέτες) για την μετάλλαξη γάμμα [36].
Σε σύγκριση με την αποτελεσματικότητα έναντι της άλφα, η μετάλλαξη δέλτα έδειξε μειωμένη αποτελεσματικότητα του εμβολίου κατά 88% για την πρόληψη της λοίμωξης για το εμβόλιο BNT162b2 (Pfizer mRNA) και κατά 67% για το εμβόλιο ChAdOx1 (AstraZeneca) [37]. Η έλλειψη συσχέτισης μεταξύ της εμβολιαστικής κάλυψης στις πολιτείες των ΗΠΑ καθώς και σε χώρες του κόσμου και η μαζική εξάπλωση της μετάλλαξης δέλτα παγκοσμίως, επίσης, συνηγορεί υπέρ μιας σημαντικά περιορισμένης αποτελεσματικότητας του εμβολίου κατά της δέλτα. Ακόμη και η πολύ υψηλή εμβολιαστική κάλυψη του πληθυσμού δεν μπόρεσε να αποτρέψει την εξάπλωση της μετάλλαξης δέλτα, καθώς πολλοί εμβολιασμένοι μολύνθηκαν και αυτοί και μετέδωσαν τη μόλυνση [38].
Σε σύγκριση με την μετάλλαξη δέλτα, μια μεγάλη βρετανική μελέτη παρατήρησης κατέδειξε σημαντικά μειωμένη αποτελεσματικότητα του εμβολίου όσον αφορά την μετάλλαξη όμικρον. Για το εμβόλιο ChAdOx1 (AstraZeneca), καμία επίδραση δεν ήταν ανιχνεύσιμη 20 εβδομάδες μετά τον δεύτερο εμβολιασμό. Δύο έως τέσσερις εβδομάδες μετά τον δεύτερο εμβολιασμό, το BNT162n2 (Pfizer) εξακολουθούσε να παρουσιάζει αποτελεσματικότητα του εμβολίου 65,5%, αλλά αυτή έπεσε κάτω από το 10% μετά από 25 εβδομάδες [39].
Συμπέρασμα: Στο βαθμό που έχει μελετηθεί – δεν υπάρχουν αξιόπιστα στοιχεία μελετών για όλα τα εμβόλια – η αποτελεσματικότητα των διαθέσιμων εμβολίων μειώνεται σημαντικά με την αύξηση της απόστασης των μεταλλάξεων από τον αρχικό τύπο Wuhan. Επιπλέον, παρατηρείται ταχεία μείωση της αρχικά επιτεύξιμης μερικής ανοσίας.
4.6-Αποτελεσματικότητα του εμβολίου σε παιδιά και εφήβους
Για τον εμβολιασμό των παιδιών (5-11 ετών) και των εφήβων (12-17 ετών), μόνο τα δύο εμβόλια mRNA (BNT162b2 [Comirnaty®] και mRNA-1273 [Spikevax®]) έχουν λάβει άδεια κυκλοφορίας στην Ευρώπη. Ωστόσο, υπάρχει επίσης μόνο μια χρονικά περιορισμένη, υπό όρους έγκριση για τα παιδιά. Όπως και για την έγκριση των εμβολίων COVID για ενήλικες, αντίστοιχες μελέτες έγκρισης πραγματοποιήθηκαν επίσης για παιδιά και εφήβους, οι οποίες, ωστόσο, είναι ακόμη λιγότερο πειστικές από τις μελέτες έγκρισης για ενήλικες λόγω μικρότερου αριθμού περιπτώσεων και μικρότερων περιόδων παρατήρησης [40-43].
Για παράδειγμα, η βασική δοκιμή του BNT162b2 (Pfizer) μελέτησε μόνο 2.268 παιδιά, εκ των οποίων 1.517 έλαβαν BNT162b2 και 751 εικονικό φάρμακο [43]. Ο διάμεσος χρόνος παρατήρησης ήταν μόλις 2,3 μήνες. Υπήρξαν 16 περιπτώσεις COVID στην ομάδα εικονικού φαρμάκου και τρεις στην ομάδα BNT162b2 τουλάχιστον επτά ημέρες μετά τη δεύτερη δόση εμβολιασμού. Από τα στοιχεία αυτά, οι συγγραφείς υπολόγισαν προσαρμοσμένη αποτελεσματικότητα του εμβολίου 90,7% (95% CI 67,7-98,3%). Σοβαρές ασθένειες, εισαγωγές στο νοσοκομείο και θάνατοι δεν παρατηρήθηκαν ούτε στην ομάδα εμβολιασμένων ούτε στην ομάδα εικονικού φαρμάκου. Ως περαιτέρω ένδειξη της αποτελεσματικότητας του εμβολίου, οι συγγραφείς θεωρούν ότι στα παιδιά επιτεύχθηκαν παρόμοιοι υψηλοί αριθμοί αντισωμάτων με αυτούς που επιτεύχθηκαν στην ομάδα 16 έως 25 ετών από την κεντρική μελέτη για τους ενήλικες.
Τα έγκυρα δεδομένα μελετών σχετικά με την αποτελεσματικότητα του εμβολίου σε παιδιά μετά την εισαγωγή του στην αγορά είναι ελάχιστα. Μια αναδρομική μελέτη κοόρτης από το Ισραήλ διαπίστωσε αποτελεσματικότητα του εμβολίου >90% για το BNT162b2 σε εφήβους σε σχέση με μια θετική για το τεστ PCR “μόλυνση”. Δεν συλλέχθηκαν κλινικά δεδομένα (συμπτώματα, ποσοστό νοσηλείας), με αποτέλεσμα το αποτέλεσμα της μελέτης να μην μπορεί να χρησιμοποιηθεί για σύσταση εμβολιασμού [44].
Σε μια μεθοδολογικά ανεπαρκή μελέτη ελέγχου περιπτώσεων, 1.185 νοσηλευόμενα παιδιά και έφηβοι με συμπτώματα τύπου COVID και θετικά αποτελέσματα PCR ή αντιγόνου συγκρίθηκαν με 1.627 αρνητικούς εθελοντές με ή χωρίς συμπτώματα COVID [45]. Από τα κρούσματα COVID, 142 (12%) είχαν εμβολιαστεί διπλά, ενώ από τους εθελοντές 592 (36%). Από τις αναλογίες πιθανοτήτων (OR), οι συγγραφείς υπολόγισαν αποτελεσματικότητα του εμβολίου 92% (95% CI 89-95%) για την μετάλλαξη δέλτα και 40% (95% CI 9-60%) για την μετάλλαξη όμικρον για τους εφήβους (12-18 ετών). Στα παιδιά (5-11 ετών), η αποτελεσματικότητα του εμβολίου ήταν 68% (95% ΔΕ 42-82%) για την μετάλλαξη Omikron (αυτό δεν μπορούσε να υπολογιστεί για την Delta λόγω έλλειψης περιπτώσεων). Επίσης, σε αυτή τη μελέτη, αποκλείστηκαν όλες οι περιπτώσεις των οποίων ο δεύτερος εμβολιασμός έγινε πριν από λιγότερο από 14 ημέρες, γεγονός που διαστρεβλώνει τα δεδομένα υπέρ του εμβολιασμού. Όπως παραδέχονται οι ίδιοι οι συγγραφείς, θα πρέπει επίσης να σημειωθεί ότι ο διαχωρισμός σε περιπτώσεις και ελέγχους είναι γεμάτος με αβεβαιότητα, επειδή οι εξετάσεις αντιγόνων έχουν ιδιαίτερα χαμηλή ευαισθησία και ειδικότητα. Τα ίδια σημεία ισχύουν και για τις μεθοδολογικά παρόμοιες περαιτέρω μελέτες ελέγχου περιπτώσεων της ίδιας ομάδας συγγραφέων (“Overcoming Covid-19 Investigators”), οι οποίες επίσης κατέληξαν σε παρόμοιο αποτέλεσμα [46,47]. Πρέπει μάλιστα να υποτεθεί ότι και στις τρεις μελέτες διερευνήθηκαν επικαλυπτόμενες συλλογικότητες ασθενών και ότι πρόκειται επομένως τουλάχιστον εν μέρει για επανάληψη αποτελεσμάτων.
Σε μία προδημοσίευση που δεν έχει ακόμη αξιολογηθεί, δίνεται αρχική αποτελεσματικότητα εμβολιασμού 85% για τους νέους 12 έως 17 ετών την πρώτη εβδομάδα του Δεκεμβρίου 2021 με λοιμώξεις που προκαλούνται κυρίως από την μετάλλαξη δέλτα [48]. Το ποσοστό αυτό μειώθηκε στο 51% την τρίτη εβδομάδα του Ιανουαρίου, όταν εμφανίστηκαν σχεδόν μόνο λοιμώξεις που προκλήθηκαν από την μετάλλαξη Omikron. Για τα παιδιά ηλικίας 5 έως 11 ετών, η αποτελεσματικότητα του εμβολίου μειώθηκε την ίδια περίοδο από το αρχικό 68% σε μόλις 12%.
Όσον αφορά τη μείωση του κινδύνου νοσηλείας ως ένδειξη σοβαρής COVID, η αποτελεσματικότητα του εμβολίου ήταν 73% για τα παιδιά ηλικίας 12-17 ετών και 48% για τα παιδιά ηλικίας 5-11 ετών. Όπως και στις μελέτες για τους ενήλικες μετά την κυκλοφορία στην αγορά, υπολογίστηκαν μόνο τα συμβάντα που συνέβησαν μετά από 14 ημέρες μετά τον δεύτερο εμβολιασμό. Τα συνολικά ποσοστά νοσηλείας και οι θάνατοι δεν αναφέρονται.
Συμπέρασμα: Τα δεδομένα της μελέτης σχετικά με τον εμβολιασμό COVID των εφήβων (12-17 ετών) και ιδίως των παιδιών (5-11 ετών) είναι περιορισμένα. Η αποτελεσματικότητα του εμβολιασμού είναι πιθανώς χαμηλότερη από την αποτελεσματικότητα στους ενήλικες. Δεν υπάρχουν ισχυρά στοιχεία ότι τα συνολικά ποσοστά νοσηλείας και η συνολική θνησιμότητα σε παιδιά και εφήβους μειώνονται από τον εμβολιασμό. Μέχρι στιγμής δεν υπάρχουν διαθέσιμες μελέτες σχετικά με τις επιπτώσεις του εμβολιασμού στη Long COVID στα παιδιά.
4.7-Εμβολιασμός νοσήσαντων
Ο κίνδυνος επαναμόλυνσης, σοβαρής εξέλιξης ή θανάτου από την COVID για όσους έχουν αναρρώσει είναι χαμηλός. Σε μια πληθυσμιακή μελέτη από το Κατάρ, το ποσοστό επαναμόλυνσης των ατόμων που ανάρρωσαν ήταν <0,4%. Από τα 1.304 άτομα με επαναμόλυνση, μόνο 4 είχαν σοβαρή εξέλιξη της νόσου και κανένα δεν πέθανε [49].
Σε μια μελέτη του Αμερικανικού Κέντρου Ελέγχου Ασθενειών (CDC), τα άτομα που ανάρρωσαν είχαν χαμηλότερο ποσοστό μόλυνσης από τα εμβολιασμένα άτομα και το ποσοστό μόλυνσης των νοσήσαντων ατόμων δεν μειώθηκε περαιτέρω με πρόσθετο εμβολιασμό [50]. Δεν είναι γνωστό πόσο διαρκεί η προστασία από την ασθένεια. Τα δεδομένα παρακολούθησης από το Κατάρ καθώς και τα δεδομένα του CDC υποδηλώνουν ότι παρέχεται επαρκής προστασία για τουλάχιστον 6-12 μήνες.
Συμπέρασμα: Όσοι έχουν αναρρώσει δεν έχουν κανένα πλεονέκτημα από έναν (πρόσθετο) εμβολιασμό COVID και εκτίθενται άσκοπα στον κίνδυνο παρενεργειών του εμβολιασμού εάν το πράξουν.
4.8-Επιδράσεις του εμβολιασμού στη Long COVID
Οι μελέτες σχετικά με τον αντίκτυπο του εμβολιασμού κατά της COVID στον κίνδυνο εμφάνισης συμπτωμάτων της Long COVID είναι ακόμη περιορισμένες. Μια αναδρομική μελέτη κοόρτης που συνέκρινε 33.940 άτομα με COVID παρά τον προηγούμενο εμβολιασμό με 113.474 ανεμβολίαστα άτομα με COVID έδειξε μείωση των συμπτωμάτων Long COVID (HR 0,85, 95% CI 0,82-0,89) και των θανάτων (HR 0,66, 95% CI 0,58- 0,74) στους εμβολιασμένους [51]. Ωστόσο, η απόλυτη διαφορά κινδύνου ήταν μόνο μικρή και τα αποτελέσματα αυτής της μελέτης κοόρτης, όπως και στις μελέτες παρατήρησης που ήδη αναφέρθηκαν, αλλοιώνονται επίσης επειδή δεν λαμβάνονται υπόψη τα συμβάντα έως και 14 ημέρες μετά τον δεύτερο εμβολιασμό.
Συζητείται επίσης η επίδραση του εμβολιασμού στα συμπτώματα long Covid. Έτσι, ο εμβολιασμός οδήγησε σε μείωση των κρουσμάτων long CoVID κατά περίπου 10% σε όσους είχαν ήδη μολυνθεί με SARS-CoV-2 [52]. Ωστόσο, οι ίδιοι οι συγγραφείς ζητούν μεγαλύτερη περίοδο παρατήρησης για την επιβεβαίωση των αποτελεσμάτων.
Συμπέρασμα: Μέχρι στιγμής υπάρχουν μόνο λίγες μελέτες σχετικά με τις επιδράσεις των εμβολίων COVID στην ανάπτυξη της Long COVID. Μια μικρή μείωση του κινδύνου Long COVID από τα εμβόλια φαίνεται πιθανή. Θα πρέπει να διεξαχθούν μεγαλύτερες μελέτες υψηλής ποιότητας για την επαλήθευση του αποτελέσματος.
4.9- Προστασία από τη μολυσματικότητα και στείρα ανοσία
Η εξάλειψη ενός παθογόνου παράγοντα από έναν πληθυσμό είναι δυνατή μόνο εάν τα εμβολιασμένα άτομα όχι μόνο προστατεύονται από την ασθένεια αλλά και επιτυγχάνουν στείρα ανοσία, δηλαδή δεν μπορούν να μεταδώσουν τον ιό και έτσι δεν μολύνουν πλέον άλλα εμβολιασμένα ή μη εμβολιασμένα άτομα. Αυτή η στείρα ανοσία προφανώς δεν παράγεται από τα διαθέσιμα εμβόλια COVID.
Σε μια αμερικανική μελέτη συγκρίθηκαν οι τιμές Ct του test PCR ανεμβολίαστων και πλήρως εμβολιασμένων ατόμων με θετικά αποτελέσματα PCR. Οι τιμές Ct <25, οι οποίες θεωρούνται μέτρο υψηλού ιικού φορτίου και συνεπώς ισχυρής μολυσματικότητας, βρέθηκαν στο 68% των εμβολιασμένων και στο 63% των μη εμβολιασμένων. Μεταξύ των συμπτωματικά αρρώστων, δεν υπήρχε διαφορά μεταξύ των εμβολιασμένων και των μη εμβολιασμένων (69% έναντι 68%)- μεταξύ των ασυμπτωματικών, υπήρχε ακόμη υψηλότερο ποσοστό ατόμων με τιμή Ct <25 μεταξύ των εμβολιασμένων (82% έναντι 29%). Μολυσματικό ιικό υλικό ανιχνεύθηκε στο 88% των ανεμβολίαστων και στο 95% των εμβολιασμένων [53].
Μια βρετανική μελέτη κοόρτης διερεύνησε τα ποσοστά μόλυνσης ανεμβολίαστων και εμβολιασμένων επαφών από εμβολιασμένους και ανεμβολίαστους ασθενείς (“δευτερογενή ποσοστά προσβολής” [SAR] των εκτεθειμένων ατόμων που αναφέρονται ως συνάρτηση της κατάστασης εμβολιασμού) [54]. Από τα 126 εμβολιασμένα άτομα, 31 (24,6%) μολύνθηκαν, ενώ από τα 40 ανεμβολίαστα άτομα 15 (37,5%). Ο σχετικός κίνδυνος (δεν αναφέρεται στη μελέτη, αλλά μπορεί να υπολογιστεί από τους αριθμούς) είναι 0,66 (95% CI 0,40-1,09). Η διαφορά μεταξύ των εμβολιασμένων και των μη εμβολιασμένων είναι επομένως αριθμητικά κάπως ευνοϊκότερη για τους εμβολιασμένους, αλλά όχι στατιστικά σημαντική (p = 0,17).
Σε ένα δεύτερο βήμα, η μελέτη αυτή κάνει διάκριση μεταξύ εμβολιασμένων και μη εμβολιασμένων ασθενών. Το ποσοστό δευτερογενούς προσβολής ήταν 24,6% για τις 69 επαφές των μολυσματικών εμβολιασμένων ατόμων και 23,0% για τις 100 επαφές των μολυσματικών ανεμβολίαστων ατόμων. Ο κίνδυνος μόλυνσης ήταν επομένως αριθμητικά κάπως υψηλότερος εδώ ακόμη και για τους εμβολιασμένους από ό,τι για τους μη εμβολιασμένους, αλλά επίσης όχι σημαντικός (RR 1,07, 95% CI 0,62-1,85).
Σε μια άλλη βρετανική μελέτη, αναλύθηκαν τα ποσοστά μόλυνσης 146.243 επαφών και 108.498 μολυσμένων ασθενών με. Τις πρώτες εβδομάδες μετά τον πλήρη εμβολιασμό, δεν υπήρξε πλήρης προστασία, αλλά περίπου μείωση του ποσοστού μόλυνσης στο μισό λόγω του εμβολιασμού. Ωστόσο, η προστασία αυτή δεν ήταν πλέον ανιχνεύσιμη όσον αφορά την μετάλλαξη δέλτα για το ChAdOx1 (AstraZeneca) ήδη δώδεκα εβδομάδες μετά τον τελευταίο εμβολιασμό και ήταν μόνο περίπου 20% για το BNT162b2 [55].
Σύμφωνα με μια δανική μελέτη, τα ποσοστά μόλυνσης των εμβολιασμένων ατόμων είναι ακόμη υψηλότερα με την μετάλλαξη Omikron σε σύγκριση με την μετάλλαξη Delta (2,6 φορές υψηλότερα για τα πλήρως εμβολιασμένα άτομα και 3,7 φορές υψηλότερα για τα άτομα που έχουν λάβει την ενισχυτική) [56].
Συμπέρασμα: Κανένα από τα διαθέσιμα εμβόλια COVID δεν επιτυγχάνει στείρα ανοσία. Ωστόσο, ο ρυθμός μόλυνσης είναι προφανώς μειωμένος ιδίως τις πρώτες εβδομάδες μετά τον εμβολιασμό, ιδίως για την α- μετάλλαξη. Ωστόσο, η αποτελεσματικότητα όσον αφορά τα ποσοστά μόλυνσης μειώνεται ραγδαία με την πάροδο του χρόνου. Μετά από περίπου τρεις μήνες, δεν μπορεί να υποτεθεί ότι τα ποσοστά μόλυνσης μειώνονται σημαντικά για την μετάλλαξη δέλτα, ενώ για την μετάλλαξη όμικρον, τα ποσοστά μόλυνσης των εμβολιασμένων ατόμων είναι και πάλι υψηλότερα.
5- Παρενέργειες των εμβολιασμών COVID
Με “τηλεσκοπικές” και επιταχυνόμενες διαδικασίες έγκρισης, ακολουθήθηκαν δύο εντελώς νέοι δρόμοι για την πρόληψη των λοιμώξεων από τον SARS-CoV-2, μία φορά μέσω της εισαγωγής γενετικά τροποποιημένου mRNA στα κύτταρα του οργανισμού και μία φορά μέσω τεχνητής μόλυνσης με γενετικά τροποποιημένους ιούς-φορείς.
Η αρχή των εμβολίων mRNA βασίζεται στο γεγονός ότι γενετικά τροποποιημένο, μεταλλαγμένο (ανταλλαγή της ουραπιδίλης με ψευδοουραπιδίλη) mRNA, το οποίο κωδικοποιεί την πρωτεΐνη spike του SARS-CoV-2, εισάγεται σε ανθρώπινα κύτταρα συσκευασμένο σε νανοσωματίδια λιπιδίων και χρησιμοποιεί τον κανονικό κυτταρικό μεταβολισμό για την παραγωγή της πρωτεΐνης spike. Στη συνέχεια προσφέρεται ή απελευθερώνεται στην επιφάνεια των κυττάρων, προκαλώντας την ενεργοποίηση του ανοσοποιητικού συστήματος κατά της πρωτεΐνης spike.
Για τα εμβόλια που βασίζονται στον ιό-φορέα, οι αδενοϊοί που είναι απαθογόνοι για τον άνθρωπο και προέρχονται από χιμπατζήδες είναι συνήθως γενετικά τροποποιημένοι ώστε να παράγουν πρωτεΐνη spike όταν οι αδενοϊοί εισβάλλουν σε ανθρώπινα κύτταρα ξενιστές και “επαναπρογραμματίζουν” την παραγωγή πρωτεϊνών στο κύτταρο. Αυτό οδηγεί επίσης στην παρουσίαση αντιγόνων της πρωτεΐνης spike στην επιφάνεια των ανθρώπινων κυττάρων ή στην απελευθέρωση της πρωτεΐνης spike και, συνεπώς, σε ανοσολογική απόκριση.
Λόγω του νέου τρόπου δράσης των εμβολίων mRNA και φορέων, εκτός από μελέτες in vitro και μελέτες σε κυτταροκαλλιέργειες, δεν υπάρχει σχεδόν καμία εμπειρία σχετικά με τον πραγματικό τρόπο δράσης και τις πιθανές ανεπιθύμητες ενέργειες. Πάνω απ’ όλα, βέβαια, δεν μπορεί παρά να υπάρχει ανεπαρκής μεσοπρόθεσμη εμπειρία και καθόλου μακροπρόθεσμη εμπειρία. Η τεχνολογία mRNA εφευρέθηκε πριν από περίπου 30 χρόνια και έχει χρησιμοποιηθεί με πολύ περιορισμένη επιτυχία στη θεραπεία κακοήθων όγκων. Ωστόσο, οι μακροχρόνιες επιδράσεις και οι πολύ σπάνια εμφανιζόμενες σοβαρές παρενέργειες δεν μπόρεσαν να διερευνηθούν λόγω του περιορισμένου αριθμού περιπτώσεων και της περιορισμένης περιόδου παρατήρησης στη θεραπεία ατόμων με καρκίνο τελικού σταδίου.
Επομένως, μπορεί να υποτεθεί κατ’ αρχήν ότι τα εμβόλια mRNA και φορέων κατά του COVID θα χρησιμοποιηθούν πειραματικά ως μαζικά εμβόλια. Για το λόγο αυτό, ο Ευρωπαϊκός Οργανισμός Φαρμάκων (ΕΜΑ) έχει εγκρίνει μόνο υπό όρους όλα τα εμβόλια COVID (“άδεια κυκλοφορίας υπό όρους”). Η έγκριση δόθηκε έτσι λόγω της μεγάλης ανάγκης για τον περιορισμό της πανδημίας, παρόλο που δεν υποβλήθηκαν επαρκή δεδομένα (ασφάλειας) για πλήρη έγκριση [57]. Μεγάλο μέρος της γνώσης σχετικά με την ασφάλεια των εμβολίων αποκτήθηκε και εξακολουθεί να αποκτάται μόνο κατά τη διάρκεια της μαζικής χρήσης των εμβολίων στον πληθυσμό, αλλά δυστυχώς μόνο από αναδρομικές μελέτες παρατήρησης, καθώς δεν είχαν ξεκινήσει τυχαιοποιημένες ελεγχόμενες δοκιμές και μελέτες κοόρτης με μεγάλο αριθμό περιστατικών όταν καθιερώθηκε ο εμβολιασμός.
5.1-Παρενέργειες στις μελέτες καταχώρισης
Στη μελέτη καταχώρισης για το Comirnaty® (BNT162b2, Pfizer/BioNTech), το 66-83% των εμβολιασθέντων παραπονέθηκε για πόνο γύρω από την ένεση (εικονικό φάρμακο <10%), ανάλογα με την ηλικία και τη δόση [13]. Το 34-59% εμφάνισε κόπωση και το 25-52% ανέφερε πονοκέφαλο. Άλλες λιγότερο συχνά αναφερόμενες ανεπιθύμητες ενέργειες ήταν πυρετός, ρίγη, διάρροια, μυϊκός και αρθρικός πόνος. Σοβαρές ανεπιθύμητες ενέργειες αναφέρθηκαν σπάνια στην αρχική δημοσίευση (σε ποσοστό 0,3%) και δεν διέφεραν σημαντικά από το εικονικό φάρμακο.
Σύμφωνα με τη μελέτη καταχώρισης, το Spikevax® οδήγησε σε τοπικές αντιδράσεις στην περιοχή της ένεσης στο 84,2-88,6% των εμβολιασθέντων (εικονικό φάρμακο 18,8-19,8%) και σε συστηματικές ανεπιθύμητες ενέργειες στο 54,9-79,4% (εικονικό φάρμακο 36,5- 42,2%) [14]. Σύμφωνα με την αρχική δημοσίευση, σοβαρές ανεπιθύμητες ενέργειες εμφανίστηκαν στο 0,6% των εμβολιασθέντων. Παρόλο που η συχνότητα των σοβαρών ανεπιθύμητων συμβάντων στην εμβολιασμένη ομάδα δεν διέφερε σημαντικά από την ομάδα ελέγχου, ένα ποσοστό 6 ανά 1.000 σοβαρές ανεπιθύμητες παρενεργειών φαίνεται πολύ υψηλή.
Εν τω μεταξύ, έχει δημοσιευθεί μια ανεξάρτητη δευτερογενής ανάλυση των δεδομένων από τις μελέτες καταχώρισης των εμβολίων mRNA, η οποία, ωστόσο, είναι διαθέσιμη μόνο ως προδημοσίευση χωρίς αξιολόγηση από ομοτίμους. Σε αυτή τη δευτερογενή ανάλυση συμπεριλήφθηκαν δεδομένα από τις βασικές μελέτες και τα δεδομένα που υποβλήθηκαν στον FDA, προκειμένου να αξιολογηθούν ρητά τα σοβαρά ανεπιθύμητα συμβάντα (SAE) και τα ανεπιθύμητα συμβάντα ειδικού ενδιαφέροντος (AESI). Στη συνδυασμένη ανάλυση και των δύο βασικών δοκιμών, τόσο τα SAE όσο και τα AESI εμφανίστηκαν συχνότερα στην ομάδα εμβολιασμένων από ό,τι στην ομάδα εικονικού φαρμάκου (σχετικός κίνδυνος για SAE 1,15, 95% CI 0,96-1,38, μη σημαντικός, κίνδυνος για AESI 1,43, 95% CI 1,07-1,92, σημαντικός). Σε απόλυτους αριθμούς, 12,9 περισσότερες SAE ανά 10.000 εμβολιασθέντες και 12,5 περισσότερες AESI ανά 10.000 εμβολιασθέντες εμφανίστηκαν μεταξύ των εμβολιασθέντων. Ο απόλυτος κίνδυνος για SAE και AESI συγκρίθηκε με την απόλυτη μείωση του κινδύνου για νοσηλεία που σχετίζεται με την COVID, η οποία ήταν 2,3/10.000 (Pfizer) και 6,4/10.000 (Moderna). Οι συγγραφείς καταλήγουν στο συμπέρασμα ότι το ισοζύγιο οφέλους/βλάβης των εμβολίων μπορεί να είναι αρνητικό [58].
Στις τέσσερις μελέτες καταχώρησης για το Vaxzevria® (AstraZeneca), οι ανεπιθύμητες ενέργειες αναφέρονται πολύ ελλιπώς. Σοβαρές ανεπιθύμητες ενέργειες εμφανίστηκαν στο 0,7% των ατόμων που εμβολιάστηκαν με το Vaxzevria®. Δεδομένου ότι η ομάδα ελέγχου (0,6% σοβαρές ανεπιθύμητες ενέργειες) εμβολιάστηκε κατά του μηνιγγιτιδόκοκκου, δεν υπάρχει σύγκριση με εικονικό φάρμακο [15].
Το εμβόλιο φορέα Jcovden® της Johnson&Johnson οδήγησε σε σοβαρές παρενέργειες στο 0,4% των εμβολιασθέντων (εικονικό φάρμακο επίσης 0,4%) [16], αλλά τα θρομβοεμβολικά επεισόδια εμφανίστηκαν πολύ συχνότερα στους εμβολιασθέντες από ό,τι με το εικονικό φάρμακο (11 έναντι 3 περιπτώσεων σε περίπου 21.000 συμμετέχοντες που αξιολογήθηκαν ανά ομάδα).
Για το πιο πρόσφατα εγκεκριμένο εμβόλιο, το Nuvaxovid® (Novavax), οι τοπικές ανεπιθύμητες ενέργειες αναφέρθηκαν ελαφρώς λιγότερο συχνά (58,0-78,9% στους εμβολιαζόμενους και 21,1- 21,7% στο εικονικό φάρμακο) και οι συστηματικές σοβαρές ανεπιθύμητες ενέργειες αναφέρθηκαν ελαφρώς συχνότερα (2,4-12,1% στους εμβολιαζόμενους, 2,1% στο εικονικό φάρμακο) μετά από δύο μήνες παρατήρησης [17].
Όταν εξετάζονται οι μελέτες καταχώρισης συνολικά, είναι εντυπωσιακή η εξαιρετικά μεγάλη διασπορά των ποσοστών παρενεργειών κάτω από το εικονικό φάρμακο (μεταξύ 0,3% για το Comirnaty® και 2,1% για το Nuvaxovid®), γεγονός που καθιστά αμφίβολη την εγκυρότητα της καταγραφής των παρενεργειών στις μελέτες.
Πολύ παρόμοιες έντονες ανεπιθύμητες ενέργειες εμφανίζονται επίσης μετά τον εμβολιασμό κατά της γρίπης, έτσι ώστε να αποτελεί καλή επιλογή για τη σύγκριση των συχνοτήτων. Σύμφωνα με μια ανασκόπηση του Cochrane που δημοσιεύθηκε το 2018, μετά τον εμβολιασμό κατά της γρίπης, τοπικές αντιδράσεις όπως ερυθρότητα ή οίδημα στην περιοχή της ένεσης εμφανίζονται κατά μέσο όρο σχεδόν στο 60% όλων των εμβολίων που αξιολογήθηκαν στην ανασκόπηση, πονοκέφαλος στο 16,5% και κόπωση στο 14,8% [59]. Αυτές οι ανεπιθύμητες ενέργειες εμφανίζονται συνεπώς σημαντικά συχνότερα με τα εμβόλια COVID.
Όλες οι μελέτες έγκρισης έχουν κοινό χαρακτηριστικό ότι οι περίοδοι παρατήρησης είναι πολύ σύντομες και ο αριθμός των περιπτώσεων πολύ μικρός, με αποτέλεσμα να μην καταγράφονται οι σπάνιες παρενέργειες και εκείνες που εμφανίζονται μόνο αργότερα στην πορεία του χρόνου.
Συμπέρασμα: Οι δοκιμές καταχώρισης των εμβολίων COVID έδειξαν σημαντική μείωση της θετικής στο test PCR συμπτωματικής νόσου COVID στα εμβολιασμένα άτομα σε σύγκριση με το εικονικό φάρμακο κατά τη στιγμή της εφαρμογής, όταν δεν λαμβάνεται υπόψη ο χρόνος μεταξύ του πρώτου εμβολιασμού και 14 ημέρες μετά τον δεύτερο εμβολιασμό. Ωστόσο, δεδομένου ότι στην πραγματικότητα αυτή τη φορά δεν επηρεάζεται από κανένα εμβολιασμένο άτομο. Εάν το εμβόλιο μπορεί να “παραλειφθεί” και ο ιός έχει αλλάξει σημαντικά στο μεταξύ, τα αποτελέσματα της μελέτης αντικατοπτρίζουν μια υψηλότερη αποτελεσματικότητα του εμβολίου από αυτή που υπάρχει στην πραγματικότητα σήμερα. Αυτή η αποτελεσματικότητα του εμβολίου έχει ως τίμημα πολύ υψηλά ποσοστά τοπικών και συστηματικών ανεπιθύμητων ενεργειών, τα οποία είναι σημαντικά υψηλότερα από εκείνα του εμβολιασμού κατά της γρίπης. Από τις μελέτες έγκρισης δεν μπορούν να εξαχθούν αξιόπιστα αποτελέσματα σχετικά με τη μακροπρόθεσμη ασφάλεια των εμβολιασμών COVID, επειδή οι περίοδοι παρατήρησης είναι πολύ σύντομες. Οι σπάνιες σοβαρές παρενέργειες δεν καταγράφηκαν επειδή ο αριθμός των περιπτώσεων ήταν πολύ μικρός. Επίσης, δεν μπορεί να αποκλειστεί μια σχέση με ένα ενίοτε σημαντικό ποσοστό εγκατάλειψης σε ορισμένες μελέτες. Αυτό ισχύει ιδίως για μελέτες σε ορισμένες ομάδες πληθυσμού (παιδιά, έγκυες γυναίκες).
5.2-Μεγάλη έλλειψη καταγραφής των παρενεργειών στις μελέτες παρατήρησης για την αποτελεσματικότητα των εμβολίων
Ούτε μία από τις διαθέσιμες μεγάλες μελέτες παρατήρησης της αποτελεσματικότητας των εμβολίων δεν εξετάζει τα ποσοστά ανεπιθύμητων ενεργειών. Ούτε καν το συνολικό ποσοστό νοσηλείας και η συνολική θνησιμότητα δεν αναφέρονται ως οι σημαντικότερες κλινικές παράμετροι για την ανεκτικότητα ενός φαρμάκου. Συνεπώς, από τις μελέτες αυτές δεν μπορούν να εξαχθούν συμπεράσματα σχετικά με την ασφάλεια των εμβολίων.
Σε μια μεγάλη αντιστοιχισμένη αναδρομική μελέτη, 824.828 εμβολιασμένα άτομα συγκρίθηκαν με τον ίδιο αριθμό ατόμων ελέγχου όσον αφορά την εμφάνιση περιστατικών νόσου κατά τις πρώτες 42 ημέρες μετά τον πρώτο εμβολιασμό [60]. Ο εμβολιασμός συσχετίστηκε με 3,24 φορές αυξημένο κίνδυνο μυοκαρδίτιδας (2,7 επιπλέον περιστατικά ανά 100.000 εμβολιασθέντες). Ο κίνδυνος λεμφαδενοπάθειας (RR 2,43, 78 περιστατικά/100.000) και έρπητα ζωστήρα (RR 1,43, 15,8 περιστατικά/100.000) ήταν επίσης σημαντικά αυξημένος σε όσους εμβολιάστηκαν. Οι θάνατοι και οι εισαγωγές σε νοσοκομεία δεν μελετήθηκαν.
Οι παρενέργειες που εμφανίστηκαν μόνο στην περαιτέρω πορεία μετά τη σύντομη περίοδο παρατήρησης των 42 ημερών δεν καταγράφηκαν φυσικά ούτε σε αυτή τη μελέτη.
Ένα άλλο σημαντικό πρόβλημα των μελετών είναι ότι οι περιπτώσεις ασθένειας, νοσηλείας και θανάτου ως αποτέλεσμα του εμβολιασμού σε άτομα θετικά στο τεστ PCR αξιολογούνται ως περιπτώσεις COVID και όχι ως εμβολιασμένα άτομα. Αυτό μπορεί να οδηγήσει σε σημαντική διαστρέβλωση των αποτελεσμάτων, η οποία θα μπορούσε να αποφευχθεί μόνο με κλινική εξέταση. Τα δεδομένα από τα ασφαλιστικά ταμεία που χρησιμοποιήθηκαν είναι ακατάλληλα στην περίπτωση αυτή.
Συμπέρασμα: Οι περισσότερες μελέτες μετά τη διάθεση στην αγορά επικεντρώνονται αποκλειστικά στα ειδικά για την COVID καταληκτικά σημεία του θετικού αποτελέσματος του test (ανεξάρτητα από τα κλινικά χαρακτηριστικά), της συμπτωματικής λοίμωξης, της νοσηλείας που σχετίζεται με την COVID και του θανάτου που σχετίζεται με τη COVID. Από αυτές τις μελέτες και τα δεδομένα δεν μπορούν να συναχθούν συμπεράσματα σχετικά με την ασφάλεια. Ο συνολικός αριθμός των μελετών σχετικά με τις σχετικές παρενέργειες των εμβολίων είναι πολύ περιορισμένος. Μια μελέτη κοόρτης για την καταγραφή των σχετικών με τους ασθενείς αποτελεσμάτων σε εμβολιασμένα και μη άτομα για μεγαλύτερο χρονικό διάστημα θα έπρεπε να είχε εφαρμοστεί με την εισαγωγή των εμβολίων COVID στην αγορά, αλλά παραμελήθηκε. Δεν υπάρχει καμία δικαιολογία για την παράλειψη αυτή.
5.3-Δεδομένα φαρμακοεπαγρύπνησης των κατασκευαστών
5.3.1-BNT162b2 (Comirnaty®)
Εκτός από τα δεδομένα ανεπιθύμητων ενεργειών από τη βασική μελέτη που έχει ήδη αναφερθεί παραπάνω, η Pfizer διεξάγει διάφορες μελέτες φαρμακοεπαγρύπνησης, τα (προκαταρκτικά) αποτελέσματα των οποίων μπορείτε να βρείτε στο Σχέδιο Διαχείρισης Κινδύνου του Comirnaty® (έκδοση 5.0, από τον Φεβρουάριο του 2022) [61].
Σημαντικοί εντοπισμένοι και δυνητικοί κίνδυνοι του BNT162b2 στα δεδομένα φαρμακοεπαγρύπνησης του κατασκευαστή είναι οι ακόλουθες ανεπιθύμητες ενέργειες:
- Αναφυλαξία (6.327 ύποπτες περιπτώσεις σε ενήλικες [1% του συνολικού συνόλου δεδομένων μετά την έγκριση], 39 θάνατοι).
- Μυοκαρδίτιδα (3.165 ύποπτες περιπτώσεις, 52 θάνατοι) και περικαρδίτιδα (2.482 ύποπτες περιπτώσεις, 10 θάνατοι).
- Ενισχυμένη νόσος που σχετίζεται με τον εμβολιασμό (Vaccine Associated Enhanced Disease -VAED) (9.233 ύποπτες περιπτώσεις, 1.230 θάνατοι).
Για τις ακόλουθες περιπτώσεις, δεν υπάρχουν ακόμη επαρκή δεδομένα για να εγγυηθούν την ασφάλεια του εμβολίου:
- Χρήση του Comirnaty® κατά τη διάρκεια της εγκυμοσύνης και του θηλασμού
- Χρήση του Comirnaty® σε άτομα με ανοσοκαταστολή
- Χρήση του Comirnaty® σε άτομα με συννοσηρότητα (π.χ. ΧΑΠ, σακχαρώδης διαβήτης, χρόνια νευρολογική νόσος, καρδιαγγειακή νόσος).
- Χρήση του Comirnaty® σε άτομα με αυτοάνοσα ή χρόνια φλεγμονώδη νοσήματα
- Χρήση του Comirnaty® ταυτόχρονα με άλλα εμβόλια
Επιπλέον, αναφέρεται ρητά ότι η μακροπρόθεσμη ασφάλεια του Comirnaty® είναι άγνωστη (“Η μακροπρόθεσμη ασφάλεια του εμβολίου COVID-19 mRNA είναι άγνωστη επί του παρόντος”, RMP 5.0, σ. 106). Περαιτέρω δεδομένα ασφάλειας της φάσης 3 θα έπρεπε να έχουν παρασχεθεί έως τον Δεκέμβριο του 2021 λόγω των απαιτήσεων του ΕΜΑ για “άδεια κυκλοφορίας υπό όρους”. Ωστόσο, η προθεσμία αυτή έχει παρέλθει χωρίς να συμβεί τίποτα. Τα τελικά δεδομένα από τις μελέτες φαρμακοεπαγρύπνησης θα ανακοινωθούν από την Pfizer στις 31 Δεκεμβρίου 2023.
5.3.2-Ad26.COV2.S (Jcovden®)
Η τελευταία διαθέσιμη έκδοση 3.1 (από τον Οκτώβριο του 2021) του σχεδίου διαχείρισης κινδύνων για το εμβόλιο COVID της Janssen απαριθμεί τους ακόλουθους αναγνωρισμένους και δυνητικούς κινδύνους του εμβολίου [62]:
- Αναφυλαξία και αλλεργικές αντιδράσεις (1,3 περιπτώσεις/εκατομμύριο δόσεις εμβολίου – για σύγκριση: γρίπη 0,2/εκατομμύριο)
- Ενισχυμένη νόσος που σχετίζεται με το εμβόλιο (VAED) (δεν υπάρχουν περιπτώσεις σε μελέτες μετά την κυκλοφορία του εμβολίου)
- Φλεβική θρόμβωση και θρομβοεμβολή (4.828 περιπτώσεις, θάνατοι δεν δηλώθηκαν)
- Σύνδρομο θρόμβωσης με θρομβοπενία (θρομβωτική θρομβοπενία επαγόμενη από εμβολιασμό – VITT, 264 περιπτώσεις, 42 θάνατοι)
- Σύνδρομο Guillain-Barré (107 περιπτώσεις, 1 θάνατος)
- Θρομβοπενία, ανοσολογική θρομβοπενία (284 περιπτώσεις, 4 θάνατοι)
Επιπλέον, αναφέρονται οι ακόλουθες πιθανές συστηματικές ανεπιθύμητες ενέργειες:
- Πολύ συχνή (≥1/10):
- Πονοκέφαλος
- Ναυτία
- Μυϊκός πόνος
- Κόπωση
- Συχνά (≥1/100 έως <1/10):
- Βήχας
- Πόνος στις αρθρώσεις
- Πυρετός
- Περιστασιακά (≥1/1000 έως <1/100):
- Τρόμος
- Πονόλαιμος
- Δερματικό εξάνθημα
- Μυϊκή αδυναμία
- Γενική αδυναμία
Για τις ακόλουθες περιπτώσεις, δεν υπάρχουν ακόμη επαρκή δεδομένα για να εγγυηθούν την ασφάλεια του εμβολίου:
- Χρήση του Jcovden® κατά τη διάρκεια της εγκυμοσύνης και του θηλασμού
- Χρήση του Jcovden® σε άτομα με ανοσοκαταστολή
- Χρήση του Jcovden® σε άτομα με συννοσηρότητα (π.χ. ΧΑΠ, σακχαρώδης διαβήτης, χρόνια νευρολογική νόσος, καρδιαγγειακή νόσος).
- Χρήση του Jcovden® σε άτομα με αυτοάνοσα ή χρόνια φλεγμονώδη νοσήματα
- Χρήση του Jcovden® ταυτόχρονα με άλλα εμβόλια
Επιπλέον, αναφέρεται ρητά ότι η μακροπρόθεσμη ασφάλεια του Jcovden® είναι άγνωστη (“Δεν υπάρχουν διαθέσιμα δεδομένα σχετικά με τη μακροπρόθεσμη ασφάλεια του Ad26.COV2.S”, RMP 3.1, σ. 56). Τα τελικά δεδομένα από τις μελέτες φαρμακοεπαγρύπνησης θα ανακοινωθούν από την Janssen στις 31 Δεκεμβρίου 2023.
5.3.3-NVX-CoV2373 (Nuvaxovid®)
Το σχέδιο διαχείρισης κινδύνου για το NVX-CoV2373 του Δεκεμβρίου 2021 υποδεικνύει μόνο πιθανούς κινδύνους, καθώς δεν υπάρχουν ακόμη διαθέσιμα δεδομένα για το Nuvaxovid μετά την κυκλοφορία [63]:
- Ενισχυμένη νόσος που σχετίζεται με το εμβόλιο (VAED)
- Αναφυλαξία
- Μυοκαρδίτιδα και περικαρδίτιδα
Λόγω έλλειψης δεδομένων, δεν μπορούν να δοθούν ακόμη πληροφορίες για τη συχνότητα. Δεν υπάρχουν επίσης διαθέσιμα στοιχεία για τους ακόλουθους τομείς εφαρμογής, οπότε δεν μπορούν να αποκλειστούν οι κίνδυνοι για την ασφάλεια:
- Χρήση του Nuvaxovid® κατά τη διάρκεια της εγκυμοσύνης και του θηλασμού
- Χρήση του Nuvaxovid® σε άτομα με ανοσοκαταστολή
- Χρήση του Nuvaxovid® σε άτομα με συννοσηρότητα (π.χ. ΧΑΠ, σακχαρώδης διαβήτης, χρόνια νευρολογική νόσος, καρδιαγγειακή νόσος).
- Χρήση του Nuvaxovid® σε άτομα με αυτοάνοσα ή χρόνια φλεγμονώδη νοσήματα
- Χρήση του Nuvaxovid® ταυτόχρονα με άλλα εμβόλια
Επιπλέον, αναφέρεται ρητά ότι η μακροπρόθεσμη ασφάλεια του Nuvaxovid® είναι άγνωστη (“Δεδομένης της φύσης του προγράμματος κλινικής ανάπτυξης του NVX-CoV2373, η κατανόηση του μακροπρόθεσμου προφίλ ασφάλειας του NVX-CoV2373 είναι επί του παρόντος περιορισμένη”, RMP 1.0, σ. 33). Τα τελικά δεδομένα της μελέτης φαρμακοεπαγρύπνησης θα ανακοινωθούν από τη Novavax στις 31 Δεκεμβρίου 2022.
5.3.4-mRNA-1273 (Spikevax®)
Η τρέχουσα έκδοση 3.0 (από τον Δεκέμβριο του 2021) του σχεδίου διαχείρισης κινδύνων για το Spikevax® απαριθμεί τους ακόλουθους αναγνωρισμένους και δυνητικούς κινδύνους από το εμβόλιο [64]:
- Αναφυλαξία (1.214 περιπτώσεις, 0,23 περιπτώσεις/100.000 δόσεις εμβολίου, θάνατοι δεν αναφέρθηκαν).
- Ενισχυμένη νόσος που σχετίζεται με το εμβόλιο (VAED, δεν έχουν αναφερθεί περιπτώσεις)
- Μυοκαρδίτιδα (362 περιπτώσεις, 3,45 περιπτώσεις/100.000 ανθρωποέτη, θάνατοι δεν αναφέρθηκαν).
- Περικαρδίτιδα (2,16 περιπτώσεις/100.000 ανθρωποέτη, αριθμός περιπτώσεων δεν αναφέρεται).
Σημαντικοί κίνδυνοι για τους οποίους δεν υπάρχει επαρκής ενημέρωση είναι:
- Χρήση του Spikevax® κατά τη διάρκεια της εγκυμοσύνης και του θηλασμού
- Χρήση του Spikevax® σε άτομα με ανοσοκαταστολή
- Χρήση του Spikevax® σε άτομα με συννοσηρότητα (π.χ. ΧΑΠ, σακχαρώδης διαβήτης, χρόνια νευρολογική νόσος, καρδιαγγειακή νόσος).
- Χρήση του Spikevax® σε άτομα με αυτοάνοσα ή χρόνια φλεγμονώδη νοσήματα
- Χρήση του Spikevax® ταυτόχρονα με άλλα εμβόλια
Για το Spikevax, επίσης, ο κατασκευαστής παραδέχεται ότι δεν υπάρχουν επαρκή δεδομένα για να γίνουν δηλώσεις σχετικά με τη μακροπρόθεσμη ασφάλεια (“Το μακροπρόθεσμο προφίλ ασφάλειας πρέπει να χαρακτηριστεί”, RMP 3.0, σ. 62). Τα τελικά δεδομένα από τις μελέτες φαρμακοεπαγρύπνησης θα είναι διαθέσιμα από τη Novavax την 1η Νοέμβριου 2022.
5.3.5-ChAdOx1-S (Vaxzevria®)
Η έκδοση 4.2 (από τον Ιούνιο του 2021) του σχεδίου διαχείρισης κινδύνων για το εμβόλιο COVID της AstraZeneca απαριθμεί τους ακόλουθους αναγνωρισμένους και δυνητικούς κινδύνους του εμβολίου [65]:
- Αναφυλαξία και αλλεργικές αντιδράσεις (πολύ σπάνια, δεν υπάρχουν στοιχεία)
- Ενισχυμένη νόσος που σχετίζεται με το εμβόλιο (VAED) (δεν υπάρχουν περιπτώσεις σε μελέτες μετά την κυκλοφορία του εμβολίου)
- Φλεβική θρόμβωση και θρομβοεμβολή (πολύ σπάνια, δεν υπάρχουν στοιχεία)
- Σύνδρομο θρόμβωσης με θρομβοπενία (VITT – θρομβοπενία που προκαλείται από εμβολιασμό, πολύ σπάνια, δεν υπάρχουν διαθέσιμα στοιχεία)
- Σύνδρομο Guillain-Barré (πολύ σπάνιο, μεμονωμένοι θάνατοι, δεν υπάρχουν στοιχεία)
- Ανοσολογικά μεσολαβούμενες νευρολογικές παθήσεις, π.χ. εγκάρσια μυελίτιδα (πολύ σπάνια, δεν υπάρχουν διαθέσιμα στοιχεία)
- Θρομβοπενία, ανοσολογική θρομβοπενία (<0,1% των περιπτώσεων, μεμονωμένοι θάνατοι, δεν υπάρχουν στοιχεία)
Δεν υπάρχουν επαρκή δεδομένα ασφαλείας για τις ακόλουθες εφαρμογές:
- Χρήση του Vaxzevria® κατά τη διάρκεια της εγκυμοσύνης και του θηλασμού
- Χρήση του Vaxzevria® σε άτομα με ανοσοκαταστολή
- Χρήση του Vaxzevria® σε άτομα με συννοσηρότητα (π.χ. ΧΑΠ, σακχαρώδης διαβήτης, χρόνια νευρολογική νόσος, καρδιαγγειακή νόσος).
- Χρήση του Vaxzevria® σε άτομα με αυτοάνοσα ή χρόνια φλεγμονώδη νοσήματα
- Χρήση του Vaxzevria® ταυτόχρονα με άλλα εμβόλια
Όπως και για όλα τα άλλα εμβόλια COVID, ο κατασκευαστής δηλώνει ότι το Vaxzevria δεν διαθέτει επαρκή δεδομένα για να προβεί σε δηλώσεις σχετικά με τη μακροπρόθεσμη ασφάλεια (“η κατανόηση του μακροπρόθεσμου προφίλ ασφάλειας του AZD1222 είναι επί του παρόντος περιορισμένη”, RMP 4.2, σ. 48). Τα τελικά δεδομένα από τις μελέτες φαρμακοεπαγρύπνησης θα ανακοινωθούν από την AstraZeneca την 1η Οκτωβρίου 2023.
Συμπέρασμα: Για όλα τα εμβόλια COVID που έχουν λάβει ειδική άδεια κυκλοφορίας στην ΕΕ αναγνωρίζονται σημαντικοί κίνδυνοι για την ασφάλεια και αναφέρονται θάνατοι μετά τον εμβολιασμό. Ακόμη και αν δεν μπορεί να αποδειχθεί σε όλες τις περιπτώσεις αιτιώδης σχέση μεταξύ εμβολιασμού, παρενέργειας και θανάτου, πρέπει να υποτεθεί ότι υπάρχει ένας όχι αμελητέος κίνδυνος. Ειδικότερα, όλοι οι κατασκευαστές επισημαίνουν ότι δεν μπορούν να εξαχθούν αποτελέσματα σχετικά με τη μακροπρόθεσμη ασφάλεια. Όλοι οι κατασκευαστές παραδέχονται επίσης ότι δεν υπάρχουν επαρκή δεδομένα ασφάλειας σχετικά με τη χρήση των εμβολίων κατά τη διάρκεια της εγκυμοσύνης και του θηλασμού, σε ανοσοκατασταλμένα άτομα, σε ηλικιωμένα άτομα με συνοδά νοσήματα και σε άτομα με αυτοάνοσα και χρόνια φλεγμονώδη νοσήματα.
5.4-Καταγραφή των ανεπιθύμητων ενεργειών φαρμάκων από το Ινστιτούτο Paul Ehrlich, τον ΕΟΦ και την Ευρωπαϊκή βάση δεδομένων για τις αναφερόμενες πιθανολογούμενες ανεπιθύμητες ενέργειες φαρμάκων
5.4.1-Έκθεση ασφάλειας του Ινστιτούτου Paul Ehrlich για τα εμβόλια COVID
Η έκθεση ασφάλειας του Ινστιτούτου Paul Ehrlich (PEI) σχετικά με την εκστρατεία εμβολιασμού COVID της 5.5.2022 συνοψίζει τα αναφερόμενα δεδομένα ανεπιθύμητων ενεργειών για 172 εκατομμύρια εμβολιασμούς COVID που έγιναν στη Γερμανία μεταξύ 27.12.2020 και 31.3.2022 [2]. Κατά τη διάρκεια αυτής της περιόδου, το PEI έλαβε 296.233 αναφορές για πιθανολογούμενες ανεπιθύμητες ενέργειες (170 αναφορές ανά 100.000 δόσεις εμβολίων). Σοβαρές ανεπιθύμητες ενέργειες εμφανίστηκαν σε 20 από τις 100.000 δόσεις του εμβολίου. Σε 2.810 περιπτώσεις, η αναφερόμενη ενέργεια εμβολιασμού είχε θανατηφόρο εξέλιξη (1,6 θάνατοι ανά 100.000 δόσεις εμβολιασμού). Η αιτιώδης συνάφεια μεταξύ εμβολιασμού και ανεπιθύμητης ενέργειας ή θανάτου δεν μπορεί να συναχθεί από τα δεδομένα αναφοράς του PEI.
Ωστόσο, σύμφωνα με έρευνα των καθηγητών Arne Burkhardt και Walter Lang, η οποία έχει μέχρι στιγμής δημοσιευθεί μόνο σε δελτία τύπου, το 50% ή και περισσότεροι από τους θανάτους θα μπορούσαν να σχετίζονται αιτιωδώς με τον εμβολιασμό COVID [66].
Ιδιαίτερο ενδιαφέρον σε αυτό το πλαίσιο παρουσιάζει η σύγκριση με τις αναφορές παρενεργειών με άλλους εμβολιασμούς. Το ερώτημα αυτό απαντήθηκε για όλους τους εμβολιασμούς που πραγματοποιήθηκαν στη Γερμανία το 2004 και το 2005 [67]. Σε αυτά τα δύο χρόνια, αναφέρθηκαν στη Γερμανία 2.630 ύποπτες περιπτώσεις ανεπιθύμητων ενεργειών, εκ των οποίων 1.777 ήταν σοβαρές και 58 είχαν ως αποτέλεσμα το θάνατο. Σε σχέση με το συνολικό αριθμό δόσεων εμβολίου περίπου 70 εκατομμυρίων που χορηγήθηκαν κατά την ίδια περίοδο, το ποσοστό αναφοράς ανεπιθύμητων συμβάντων ανέρχεται σε 3 ανά 100.000 δόσεις εμβολίου και το ποσοστό θανάτων σε 0,08 ανά 100.000 δόσεις εμβολίου. Το ποσοστό αναφοράς για τα εμβόλια COVID είναι επομένως σχεδόν 60 φορές μεγαλύτερο από το ποσοστό αναφοράς για άλλα εμβόλια και 20 φορές μεγαλύτερο για το ποσοστό θανάτων.
5.4.2-Η έκθεση του ΕΟΦ
Ο Ε.Ο.Φ δημοσίευσε [103] (07.04.2022) την πρώτη ανάλυση(μετά απο 1+ χρόνο χορήγησης των εμβολίων) των δεδομένων φαρμακοεπαγρύπνησης στην Ελλάδα με τίτλο “Συγκεντρωτικά στοιχεία Ε.Ο.Φ. για αναφορές στην Ελλάδα πιθανολογούμενων ανεπιθύμητων ενεργειών εμβολίων COVID -19 από την έναρξη χορήγησης των εμβολίων στην Ελλάδα έως 26.12.2021“. Η τελευταία ανάλυση αντίστοιχων δεδομένων που έχει πραγματοποιήσει και δημοσιεύσει ο οργανισμός, ήταν το 2007 [104].
Από την έναρξη της χορήγησης των προϊόντων κατά της Covid μέχρι και τις 26.12.2021, διανεμήθηκαν συνολικά στην Ελλάδα 16.993.166 δόσεις.
Εντύπωση προκαλεί το γεγονός ότι ο ΕΟΦ αναφέρει λιγότερους θανάτους στην ανακοίνωσή του από τους θανάτους που έχει αποστείλει στον ΕΜΑ. Από τις 130 θανατηφόρες αναφορές, για περισσότερες από τις μισές (53%) έκρινε ο ΕΟΦ ότι δεν ήταν πιθανή η συσχέτισή τους με τον εμβολιασμό (unlikely). 31 (24%) αναφορές δεν ήταν δυνατό να αξιολογηθούν από τα διαθέσιμα στοιχεία που έχουν αποσταλεί (unassessable) και 23 (18%) αναφορές δεν έχει ολοκληρωθεί η αξιολόγησή τους (conditional), διότι αναμένονται συμπληρωματικά στοιχεία που έχουν ζητηθεί (π.χ πορίσματα ιατροδικαστικών εκθέσεων και άλλες πληροφορίες). 4 αναφορές αξιολογήθηκαν ότι έχουν ισχυρή πιθανότητα συσχέτισης με τον εμβολιασμό (probable) και 3 αναφορές αξιολογήθηκαν ότι έχουν πιθανότητα συσχέτισης με τον εμβολιασμό (possible).
Ανησυχητικά είναι και τα περιστατικά εμφάνισης μυοκαρδίτιδας/περικαρδίτιδας στους νέους ηλικίας 12-17 ετών. Και εκεί παρατηρούμε μια σημαντική διαφορά στα στοιχεία της ανακοίνωσης του ΕΟΦ και στα στοιχεία του ΕΜΑ. Στα δεδομένα του Ευρωπαϊκού οργανισμού παρατηρούμε οτι υπάρχουν 12 περιστατικά μυοκαρδίτιδας χωρίς αναφορά ηλικίας τα οποία όμως σύμφωνα με το πεδίο “age group reporter” μπορούμε εύκολα να εξάγουμε το συμπέρασμα ότι πρόκειται για εφήβους και παιδιά.
Επιπλέον ο ΕΟΦ δεν ασχολείται με την ηλικιακή ομάδα 0-11 ετών για την οποία υπάρχουν ήδη αρκετές αναφορές. Αρκετές από αυτές αφορούν σοβαρά περιστατικά κατά την εγκυμοσύνη (συμπεριλαμβανομένων πρόωρων τοκετών και αποβολών/διακοπών κυήσεων) για τις οποίες ο ΕΟΦ έχει λάβει 13 αναφορές. Τα δεδομένα του ΕΜΑ για την Ελλάδα αναφέρουν 14 [105].
Για τα βρέφη και τα παιδιά ηλικίας 0-11 ετών υπάρχουν 18 αναφορές στα δεδομένα του ΕΜΑ(που δεν συμπεριλαμβάνονται στη κατηγορία του ΕΟΦ με τις 13 αναφορές), τις περισσότερες από τις οποίες θα μπορούσε ένας ιατρός να τις κατατάξει στην κατηγορία των αρκετά σοβαρών.
Ο ΕΟΦ στο έγγραφό του τονίζει επίσης ότι:
Σύμφωνα με το άρθρο 4 του Κανονισμού 507/2006:
«Άδεια κυκλοφορίας υπό όρους μπορεί να χορηγηθεί όταν η επιτροπή διαπιστώνει ότι, ενώ δεν έχουν υποβληθεί εκτενή κλινικά στοιχεία σχετικά με την ασφάλεια και την αποτελεσματικότητα του φαρμάκου πληρούνται οι ακόλουθες απαιτήσεις:
• η σχέση κινδύνου-οφέλους του φαρμάκου, όπως ορίζεται στο άρθρο 1 παράγραφος 28 α της οδηγίας 2001/83/ΕΚ, είναι θετική.
• αναμένεται ότι ο αιτών θα είναι σε θέση να υποβάλει εκτενή κλινικά στοιχεία.
• καλύπτονται ανικανοποίητες ιατρικές ανάγκες.
• το όφελος για τη δημόσια υγεία από την άμεση διαθεσιμότητα στην αγορά του εν λόγω φαρμάκου είναι μεγαλύτερο από τον κίνδυνο που εμπεριέχει το γεγονός ότι απαιτούνται ακόμη συμπληρωματικά στοιχεία».
αλλά δεν αναφέρει πουθενά αν τελικά, η σχέση κινδύνου-οφέλους είναι θετική ή αρνητική.
5.4.3-Συνοπτική έκθεση ασφάλειας του ΕΜΑ
Στις 12 Μαΐου 2022, ο Ευρωπαϊκός Οργανισμός Φαρμάκων δημοσίευσε την τελευταία ενημέρωση για την ασφάλεια των εμβολίων COVID-19 [68]. Η παρούσα έκθεση παραθέτει τόσο τον αριθμό των δόσεων εμβολίου που χορηγήθηκαν όσο και τον αριθμό των ανεπιθύμητων ενεργειών και των θανάτων που αναφέρθηκαν (βλ. Πίνακα 2).
Δεδομένου ότι δεν υπάρχουν αξιόπιστες μελέτες μέχρι στιγμής, μπορεί μόνο να υποτεθεί ποιο ποσοστό των αναφερόμενων παρενεργειών και θανάτων σχετίζεται αιτιωδώς με τους εμβολιασμούς. Οι αδημοσίευτες ακόμη παθολογικές μελέτες [66], οι οποίες υποθέτουν αιτιώδη σχέση μεταξύ εμβολιασμού και θανάτου στο 50% των περιπτώσεων, μπορεί ενδεχομένως να μην χαρακτηριστούν αντιπροσωπευτικές εδώ, αλλά καθιστούν σαφές ότι υπάρχει επείγουσα ανάγκη για έρευνα.
| Εμβόλιο | Αριθμός δόσεων εμβολίου | Αναφερόμενες παρανέργειες | Ποσοστό παρενεργειών/1000 δόσεις εμβολίου | Αναφερόμενοι θάνατοι | Ποσοστό θνησιμότητας/100.000 δόσεις εμβολίου |
| Comirnaty® | 627.000.000 | 743.735 | 1,19 | 7.765 | 1,2 |
| Jcovden® | 19.400.000 | 48.410 | 2,50 | 311 | 1,6 |
| Nuvaxovid® | 178.000 | 294 | 1,65 | 0 | 0,0 |
| Spikevax® | 155.000.000 | 206.920 | 1,33 | 1.025 | 0,7 |
| Vaxzevria® | 69.000.000 | 276.697 | 4,01 | 1.529 | 2,2 |
| Σύνολο | 870.578.000 | 1.276.056 | 1,47 | 10.630 | 1,2 |
Συμπέρασμα: Παρόλο που η αιτιώδης συνάφεια μεταξύ του εμβολιασμού και των αναφερόμενων παρενεργειών του εμβολιασμού ή των θανάτων σε διαχρονική σχέση με τον εμβολιασμό δεν είναι βέβαιη, είναι εντυπωσιακό ότι το ποσοστό αναφοράς και ιδίως το ποσοστό θανάτων είναι πολλαπλάσια από τα ποσοστά για άλλα εμβόλια. Συνεπώς, τα εμβόλια COVID είναι πολύ πιθανό να είναι σημαντικά λιγότερο ανεκτά από τα συμβατικά εμβόλια. Τα διαθέσιμα δεδομένα δείχνουν ότι ο κίνδυνος θανάτου είναι έως και 20 φορές αυξημένος σε σύγκριση με άλλα εμβόλια.
5.5-Ειδικές παρενέργειες εμβολιασμού των εμβολίων COVID και των Red Hand Letters
Ενώ οι μελέτες καταγραφής ανέφεραν σε γενικές γραμμές παρενέργειες χωρίς σοβαρές συνέπειες για το εμβολιαζόμενο άτομο, υπάρχουν αυξανόμενες ενδείξεις από μεμονωμένες αναφορές περιπτώσεων και δεδομένα φαρμακοεπαγρύπνησης ότι ορισμένες ανεπιθύμητες ενέργειες εμφανίζονται με δυσανάλογα μεγάλη συχνότητα.
Εν τω μεταξύ, εννέα επιστολές „Red Hand“ έχουν δημοσιευθεί από τους κατασκευαστές εμβολίων, επισημαίνοντας σημαντικές σοβαρές παρενέργειες των εμβολίων COVID (https://www.pei.de/DE/newsroom/veroffentlichungen-arzneimittel/rote-hand-briefe/rote-hand-briefenode.html).
Αυτές οι παρενέργειες των εμβολίων COVID ονομάζονται επίσης ανεπιθύμητες ενέργειες ειδικού ενδιαφέροντος. Αυτές περιλαμβάνουν:
5.5.1-Μυοκαρδίτιδα και περικαρδίτιδα
Η αυξημένη επίπτωση μυοκαρδίτιδας και περικαρδίτιδας μετά τον εμβολιασμό με ένα από τα δύο εμβόλια mRNA είναι πλέον αδιαμφισβήτητη. Σύμφωνα με μια μεγάλη αναδρομική μελέτη κοόρτης από το Ισραήλ, ο κίνδυνος μυοκαρδίτιδας είναι υπερτριπλάσιος μετά τον εμβολιασμό με BNT162b2 [60]. Ωστόσο, ο κίνδυνος μυοκαρδίτιδας είναι επίσης αυξημένος στη συμπτωματική νόσο COVID, έως και 18 φορές. Και πάλι, τονίζεται η σχετική αύξηση του κινδύνου για να δοθεί η εντύπωση υψηλού κινδύνου. Μια 18πλάσια αύξηση σε απόλυτους όρους σημαίνει μόνο 11 επιπλέον περιπτώσεις ανά 100.000 περιπτώσεις COVID σε σύγκριση με 100.000 άτομα χωρίς COVID [60]. Μια άλλη μεγάλη αναδρομική μελέτη κοόρτης δεν διαπίστωσε καθόλου αυξημένο κίνδυνο για μυοκαρδίτιδα ή περικαρδίτιδα στους ανεμβολίαστους πάσχοντες από COVID σε σύγκριση με τους μη πάσχοντες (προσαρμοσμένη αναλογία κινδύνου 1,08, 95% CI 0,45-2,56 για μυοκαρδίτιδα και 0,53, 95% CI 0,25-1,13 για περικαρδίτιδα [69].
Σε μια αγγλική μελέτη εξετάστηκαν οι απόλυτοι αριθμοί. Οι συγγραφείς υπολογίζουν 1-10 επιπλέον περιπτώσεις μυοκαρδίτιδας ανά 100.000 εμβολιασμένα άτομα, αλλά και 40 επιπλέον περιπτώσεις ανά 100.000 περιπτώσεις COVID [70]. Ειδικά όταν συγκρίνεται ο κίνδυνος συνοδού νόσου ως αποτέλεσμα του εμβολιασμού ή ως αποτέλεσμα φυσικής μόλυνσης, πρέπει φυσικά να λαμβάνεται υπόψη ότι μόνο ένα κλάσμα του πληθυσμού νοσεί, ενώ σχεδόν το σύνολο του πληθυσμού πρόκειται να εμβολιαστεί. Στη Γερμανία, από την έναρξη της πανδημίας SARS-CoV-2 τον Φεβρουάριο του 2020 έως σήμερα, περίπου 26 εκατομμύρια άνθρωποι έχουν βρεθεί θετικοί σε SARS-CoV-2, δηλαδή κατά μέσο όρο περίπου 6 εκατομμύρια ανά εξάμηνο. Έτσι, εάν ο εμβολιασμός απαιτείται κάθε έξι μήνες, 10 φορές περισσότεροι άνθρωποι θα εμβολιαστούν από όσους θα προσβληθούν από την COVID. Επομένως, η εμβολιασμένη μυοκαρδίτιδα θα εμφανίζεται επίσης 10 φορές πιο συχνά, έτσι ώστε ακόμη και αν η μυοκαρδίτιδα είναι 5 φορές πιο συχνή υπό τη νόσο από ό,τι μετά τον εμβολιασμό, θα υπάρχουν και πάλι πολύ περισσότερες περιπτώσεις μυοκαρδίτιδας που προκλήθηκε από εμβολιασμό.
Η μυοκαρδίτιδα που προκαλείται από εμβολιασμό είναι πιθανώς υπεύθυνη για πολυάριθμους θανάτους σε διαχρονική συσχέτιση με τον εμβολιασμό. Οι μελέτες αυτοψίας αποκάλυψαν ένα τυπικό ιστοπαθολογικό πρότυπο που διαφέρει σημαντικά από τη συνήθη ιστολογία της μυοκαρδίτιδας [71]. Μια συστηματική ανασκόπηση ανέφερε θνησιμότητα 1,1% για μυοκαρδίτιδα από το εμβόλιο COVID [72]. Η μακροπρόθεσμη έκβαση μετά από μυοκαρδίτιδα αναφέρεται με διαφορετικό τρόπο στη βιβλιογραφία ανάλογα με τη μεθοδολογία. Σε μια αναδρομική μελέτη περιπτώσεων, η συνολική θνησιμότητα σε 5 έτη ήταν 4,4% [73]. Σε μια μεγάλη αναδρομική μελέτη κοόρτης για 8,5 έτη παρακολούθησης διαπιστώθηκε συνολική θνησιμότητα 21,9 ανά 1.000 έτη ασθενών [74]. Υπάρχει επείγουσα ανάγκη για περαιτέρω έρευνα σχετικά με τη μακροπρόθεσμη πρόγνωση της μυοκαρδίτιδας και ειδικότερα της μυοκαρδίτιδας που προκαλείται από το εμβόλιο COVID. Ωστόσο, καθίσταται ήδη σαφές ότι θα πρέπει να αναμένονται σημαντικές επακόλουθες ζημιές, ακόμη και θάνατοι, ακόμη και μετά από μεγάλα χρονικά διαστήματα.
5.5.2-Παράλυση προσώπου
Μια σύνδεση μεταξύ του εμβολιασμού COVID και της εμφάνισης παράλυσης του προσωπικού νεύρου φαίνεται πιθανή με βάση πολυάριθμες αναφορές περιπτώσεων. Ωστόσο, δεν υπάρχουν αξιόπιστα δεδομένα μελέτης που να αποδεικνύουν ότι ο εμβολιασμός COVID σχετίζεται με αυξημένο κίνδυνο παράλυσης του προσωπικού νεύρου. Μια ανασκόπηση συνοψίζει τα διαθέσιμα στοιχεία, τα οποία βασίζονται μόνο σε αναφορές περιπτώσεων και μικρές μελέτες ελέγχου περιπτώσεων. Η αυξημένη συχνότητα εμφάνισης παράλυσης του προσωπικού νεύρου στο πλαίσιο της COVID αναλύεται επίσης [75].
5.5.3-Θρομβωτικό-θρομβοπενικό σύνδρομο
Η επαγόμενη από τον εμβολιασμό θρομβοπενία (VITT) είναι γνωστή ως τυπική παρενέργεια των εμβολίων φορέων κατά της COVID (ChAdOx1 και Ad26.COV2.S). Η επίπτωση αναφέρεται ότι είναι 0,1-0,8 ανά 100.000 δόσεις εμβολίου [76]. Ο κατασκευαστής εξέδωσε σχετική επιστολή (red hand) για να ενημερώσει τους χρήστες [77].
5.5.4- Θρόμβωση Φλεβωδών Κόλπων Εγκεφάλου
Θρόμβωση των φλεβών του κόλπου έχει επίσης παρατηρηθεί σε συνδυασμό με θρομβοπενία, ιδίως μετά τη χρήση εμβολίων φορέων. Μια συστηματική ανασκόπηση επισημαίνει ότι η θρόμβωση των φλεβών του κόλπου είναι η πιο συχνή εκδήλωση θρομβοεμβολικών επιπλοκών μετά τον εμβολιασμό COVID, αντιπροσωπεύοντας το 28,3% των περιπτώσεων, και ότι η πλειονότητα των περιπτώσεων παρατηρήθηκε μετά τον εμβολιασμό Vaxzevria® [78]. Μια συστηματική ανασκόπηση με μετα-ανάλυση κατέληξε στο συμπέρασμα ότι ο κίνδυνος θρόμβωσης των φλεβών του κόλπου μετά τη χρήση του ChAdOx1 nCoV-19 (Vaxzevria®) ήταν 23/100.000, 25 φορές υψηλότερος από τον κίνδυνο υποβάθρου στον γενικό πληθυσμό (0,9/100.000) [79]. Ωστόσο, η θρόμβωση των φλεβών του κόλπου εμφανίζεται επίσης στο πλαίσιο της ασθένειας COVID και περίπου 4-6 φορές συχνότερα από ό,τι μετά τον εμβολιασμό [80]. Ωστόσο, εδώ ισχύει ό,τι και για τη μυοκαρδίτιδα: εάν 10 φορές περισσότεροι άνθρωποι εμβολιάζονται από όσους νοσούν από COVID, τότε η SVT προκαλείται συχνότερα σε απόλυτους αριθμούς από τους εμβολιασμούς παρά από τη νόσο.
5.5.5-Άλλες φλεβικές θρομβώσεις και θρομβοεμβολές
Οι φλεβικές θρομβώσεις παρατηρήθηκαν συχνότερα μετά τη χρήση του Vaxzevria® και του Jcovden®. Πρόκειται για μεμονωμένες περιπτώσεις που εμφανίστηκαν και στη μελέτη έγκρισης[16].
Αλλά και για το BNT162b2, ενδέχεται να υπάρχει ελαφρώς αυξημένος κίνδυνος κατά τις τρεις πρώτες εβδομάδες μετά τον εμβολιασμό [81]. Μια συστηματική ανασκόπηση κατέληξε στο συμπέρασμα ότι μπορεί να εμφανιστούν θρομβοεμβολικά επεισόδια σε σχέση με όλα τα εμβόλια COVID. Ωστόσο, ο κίνδυνος φαίνεται να είναι υψηλότερος για το Vaxzevria®. Μόνο δύο περιπτώσεις εμφανίστηκαν μετά το BNT162b2 και καμία μετά το mRNA1273, οπότε δεν μπορεί να γίνει καμία έγκυρη διεξαγωγή συμπεράσματος σχετικά με τα εμβόλια mRNA [78]. Ωστόσο, δεν υπάρχουν μακροχρόνιες μελέτες και επομένως είναι άγνωστο για πόσο χρονικό διάστημα μετά τον εμβολιασμό ο κίνδυνος παραμένει και πόσο υψηλός είναι πραγματικά σε μακροχρόνια πορεία.
5.5.6-Αναφυλαξία και αλλεργικές αντιδράσεις
Σύμφωνα με συστηματική ανασκόπηση, η συχνότητα αναφυλακτικών αντιδράσεων ανέρχεται σε περίπου 9 περιπτώσεις ανά εκατομμύριο δόσεις εμβολίου [82]. Συγγραφείς από τη Γερμανία υποθέτουν παρόμοια επίπτωση 1 κρούσμα ανά 100.000 δόσεις εμβολίου [83]. Επισημαίνεται ρητά ότι τα κέντρα εμβολιασμού και τα άτομα που εμβολιάζουν πρέπει να αναμένουν και να είναι προετοιμασμένα για αναφυλακτικές αντιδράσεις.
5.5.7-Έρπης ζωστήρας
Σε μια μεγάλη αναδρομική μελέτη κοόρτης, διαπιστώθηκε ότι τα άτομα που εμβολιάστηκαν κατά της COVID είχαν σχεδόν διπλάσιο κίνδυνο εμφάνισης έρπητα ζωστήρα τις πρώτες 60 ημέρες μετά τον εμβολιασμό σε σχέση με τους ανεμβολίαστους[84]. Μια μεγάλη ισραηλινή μελέτη σε πάνω από 800.000 εμβολιασμένα άτομα σε σύγκριση με ισάριθμα μη εμβολιασμένα άτομα διαπίστωσε επίσης 1,43 φορές αυξημένο κίνδυνο εμφάνισης έρπητα ζωστήρα [60].
5.5.8-Καρδιακή προσβολή και εγκεφαλικό επεισόδιο
Είναι αμφιλεγόμενο αν υπάρχει αυξημένος κίνδυνος καρδιακής προσβολής ή εγκεφαλικού επεισοδίου μετά τον εμβολιασμό με COVID. Σε μια συστηματική ανασκόπηση, από 274 περιπτώσεις που αναλύθηκαν με θρομβοεμβολικά επεισόδια μετά τον εμβολιασμό COVID, το 20,1% έπαθε έμφραγμα του μυοκαρδίου και το 8,0% εγκεφαλικό επεισόδιο [78].
Σε μια συγκριτική μελέτη ασφάλειας σε βετεράνους των ΗΠΑ (διάμεση ηλικία 69 ετών), σημειώθηκαν 10,6 επιπλέον εγκεφαλικά επεισόδια και 14,8 επιπλέον καρδιακές προσβολές ανά 10.000 εμβολιασθέντες με BNT162b2 σε σύγκριση με το mRNA-1273 κατά μέσο όρο 38 εβδομάδες μετά τον εμβολιασμό [85].
Ωστόσο, άλλες μελέτες που συνέκριναν τη συχνότητα εμφάνισης εμφράγματος του μυοκαρδίου και εγκεφαλικού επεισοδίου σε εμβολιασμένα άτομα κατά την περίοδο μετά τον εμβολιασμό με την περίοδο πριν τον εμβολιασμό ή μελέτες που συνέκριναν εμβολιασμένα με μη εμβολιασμένα άτομα, δεν διαπίστωσαν αυξημένο κίνδυνο μετά τον εμβολιασμό κατά της COVID [60,86]. Ωστόσο, οι μελέτες αυτές κατέγραψαν μόνο τις πρώτες μία έως τρεις εβδομάδες μετά τον εμβολιασμό.
Συμπέρασμα: Συνολικά, πρέπει να θεωρηθεί ότι όλα τα εμβόλια COVID συνδέονται με έναν όχι αμελητέο κίνδυνο παρενεργειών, ορισμένες από τις οποίες είναι σοβαρές. Δεν είναι διαθέσιμες τυχαιοποιημένες ελεγχόμενες μελέτες με επαρκή αριθμό περιπτώσεων και μελέτες κοορτής που να συγκρίνουν μη εμβολιασμένα και εμβολιασμένα άτομα με επαρκώς μακρά περίοδο παρακολούθησης. Επίσης, δεν υπάρχουν μακροπρόθεσμες μελέτες για την εκτίμηση περαιτέρω όψιμων επιπτώσεων των εμβολιασμών, όπως αυξημένο ποσοστό καρκίνου ή αυξημένος κίνδυνος καρδιαγγειακών επεισοδίων, όπως καρδιακή προσβολή ή εγκεφαλικό επεισόδιο.
5.6-Υποδήλωση παρενεργειών
Μια κάπως παλαιότερη συστηματική ανασκόπηση συνοψίζει μελέτες σχετικά με την αναφορά ανεπιθύμητων ενεργειών φαρμάκων [87]. Οι συγγραφείς αναφέρουν ότι κατά μέσο όρο μόνο το 6% όλων των ανεπιθύμητων ενεργειών φαρμάκων αναφέρεται. Σοβαρές ανεπιθύμητες ενέργειες φαρμάκων αναφέρονται συχνότερα (περίπου 15%), αλλά εξακολουθούν να αναφέρονται πολύ σπάνια.
Τα διαφορετικά ποσοστά αναφοράς από τις διάφορες χώρες στο Ευρωπαϊκό Κέντρο Αναφοράς Ανεπιθύμητων Ενεργειών (https://dap.ema.europa.eu/analytics/saw.dll?PortalPages ) δείχνουν ότι μόνο λίγες ανεπιθύμητες ενέργειες για τους εμβολιασμούς COVID αναφέρονται, ιδίως στη Γερμανία. Έτσι υπάρχουν 187.796 αναφορές από τη Γερμανία στη βάση δεδομένων για το BNT162b2, που αντιστοιχούν σε 1,04 αναφορές ανά 1.000 δόσεις εμβολίου. Στην Αυστρία, το ποσοστό αναφοράς είναι υπερτριπλάσιο από αυτό της Γερμανίας, με 3,53 αναφορές ανά 1.000 δόσεις εμβολίου, και των Κάτω Χωρών, με 3,75/1.000, σχεδόν τετραπλάσιο.
Η Ελλάδα, αναλογικά με τον πληθυσμό και τον αριθμό των δόσεων, κατέχει από τις τελευταίες θέσεις στην Ευρώπη όσον αφορά τις αναφορές ανεπιθύμητων ενεργειών.
| Χώρα | Πληθυσμός | Δόσεις ανά 100 κατοίκους | Αριθμός δηλωμένων ανεπιθύμητων ενεργειών (% συνολικών αναφορών) |
| Ελλάδα | 10.423.054 | 188,3 | 9.498 (~1%) |
| Ολλανδία | 17.134.872 | 195 | 206.875 (21,5%) |
| Βέλγιο | 11.589.623 | 214,8 | 25.084 (2%) |
| Πορτογαλία | 10.196.709 | 228,4 | 23.444 (3%) |
| Σουηδία | 10.099.265 | 192,6 | 32.325 (2,3%) |
| Τσεχία | 10.708.981 | 162,3 | 15.142 (~2%) |
| Ουγγαρία | 9.660.351 | 163,5 | 5.399 (~0,5%) |
| Αυστρία | 9.006.398 | 201,5 | 93.955 (9,5%) |
Συγκριτικός αριθμός αναφορών για τα 4 πειραματικά προϊόντα(συνολικά)-19.03.2022
Απο τον παραπάνω πίνακα μπορούμε εύκολα να εξάγουμε το συμπέρασμα οτι η Ελλάδα, συγκριτικά με τις υπόλοιπες χώρες, δηλώνει ελάχιστες ανεπιθύμητες ενέργειες. Η Σουηδία με αντίστοιχο πληθυσμό και ποσοστό εμβολιασμών έχει υπερτριπλάσιες ανεπιθύμητες ενέργειες από ότι η χώρα μας, η Τσεχία με λιγότερους εμβολιασμούς έχει δηλώσει σχεδόν διπλάσιο αριθμό ανεπιθύμητων ενεργειών από ότι η Ελλάδα.
Δεδομένα από τα γερμανικά εταιρικά ταμεία ασφάλισης υγείας αποκαλύπτουν, μετά από αξιολόγηση των κωδικών διάγνωσης, ότι κωδικοποιούνται έως και 10 φορές περισσότερες διαγνώσεις παρενεργειών εμβολιασμού από ό,τι αναφέρονται στο Ινστιτούτο Paul Ehrlich [4]. Εάν τα στοιχεία αυτά είναι σωστά, τότε με βάση τα στοιχεία του PEI, μπορεί να αναμένεται ένα ποσοστό 200 σοβαρών παρενεργειών ανά 100.000 δόσεις εμβολίου και ένα ποσοστό θανάτων 16 ανά 100.000 δόσεις εμβολίου ή ένας θάνατος ανά περίπου 6.000 εμβολιασμούς.
Η προφανής υποδήλωση επιβεβαιώνεται από μια δημοσίευση της Kassenärztliche Bundesvereinigung [88]. Έτσι, το 2021, 2.487.526 ασθενείς έλαβαν θεραπεία για παρενέργειες από τον εμβολιασμό COVID στον τομέα που είναι διαπιστευμένος από το υπουργείο υγείας. Για την ίδια περίοδο, η έκθεση ασφάλειας του PEI παρουσιάζει μόνο έναν αριθμό 244.576 αναφερόμενων παρενεργειών [89]. Σε σχέση με τον αριθμό των εμβολιασμένων ατόμων που ανέρχεται σε περίπου 60 εκατομμύρια στις 31.12.2021, επομένως, περίπου κάθε 24ο άτομο που έχει εμβολιαστεί με COVID έχει συμβουλευτεί γιατρό λόγω παρενέργειας. Φυσικά, ούτε η αιτιώδης συνάφεια ούτε η σοβαρότητα και η εξέλιξη μπορούν να συναχθούν από αυτά τα δεδομένα. Για το σκοπό αυτό, θα πρέπει επειγόντως να διεξαχθούν μελέτες παρακολούθησης.
Συμπέρασμα: Δεν υπάρχουν αξιόπιστα, προοπτικά συλλεγμένα δεδομένα σχετικά με την υποδήλωση ανεπιθύμητων ενεργειών στα εμβόλια COVID. Τα διαφορετικά ποσοστά αναφοράς των κρατιδίων και η εμπειρία από τη γενική υποδήλωση των ανεπιθύμητων ενεργειών των φαρμάκων αποδεικνύουν ότι μόνο ένα μέρος των ανεπιθύμητων ενεργειών του εμβολίου COVID καταγράφεται. Η υποψία αυτή επιβεβαιώνεται από τα στοιχεία των ταμείων ασφάλισης υγείας και του Ομοσπονδιακού Συλλόγου Κρατικών Ταμείων Υγείας στη Γερμανία. Συνεπώς, πρέπει να αναμένονται πολύ περισσότερες παρενέργειες και ενδεχομένως και θάνατοι απ’ ό,τι δείχνουν οι εκθέσεις ασφάλειας των κέντρων αναφοράς.
5.7-Υπερβάλλουσα θνησιμότητα που σχετίζεται με τους εμβολιασμούς COVID
Εδώ και αρκετό καιρό συζητείται μια πιθανή σχέση μεταξύ των μαζικών εμβολιασμών και της υπερβάλλουσας θνησιμότητας που παρατηρήθηκε την ίδια περίοδο [90]. Τα στοιχεία της Ομοσπονδιακής Στατιστικής Υπηρεσίας δείχνουν για τη Γερμανία ότι το 2020 η δημογραφικά προσαρμοσμένη παρατηρούμενη θνησιμότητα ήταν μόνο 0,43% υψηλότερη από την αναμενόμενη θνησιμότητα, ενώ το 2021 υπήρχε προσαρμοσμένη υπερβάλλουσα θνησιμότητα 2,81% [90]. Είναι ιδιαίτερα εντυπωσιακό ότι η υπερβάλλουσα θνησιμότητα δεν αφορά τις ηλικιακές ομάδες στις οποίες συμβαίνουν οι περισσότεροι θάνατοι από COVID, αλλά κυρίως τις νεότερες ηλικιακές ομάδες, ιδίως την ηλικιακή ομάδα 40-49 ετών (προσαρμοσμένη υπερβάλλουσα θνησιμότητα το 2021 9,02%). Η παρατήρηση αυτή συνηγορεί κατά της υπερβάλλουσας θνητότητας που οφείλεται στην COVID. Η Ομοσπονδιακή Στατιστική Υπηρεσία αναφέρει επίσης ότι οι αναφερόμενοι θάνατοι από COVID-19 μπορούν να εξηγήσουν μόνο εν μέρει τα αυξημένα ποσοστά θνησιμότητας [91]. Η διαχρονική σχέση μεταξύ της υπερβάλλουσας θνησιμότητας κατά τη διάρκεια του έτους και των εκστρατειών εμβολιασμού υποδηλώνει την αιτιώδη συνάφεια, αλλά δεν την αποδεικνύει. Οι παράπλευρες απώλειες των μέτρων περιορισμού και τις ελλείψεις εφοδιασμού και προσωπικού στο σύστημα υγείας έρχονται επίσης στο προσκήνιο ως πιθανές αιτίες. Τα στατιστικά στοιχεία για την αιτία θανάτου, τα οποία δεν είναι ακόμη διαθέσιμα λεπτομερώς για το 2021, θα παράσχουν περαιτέρω πληροφορίες σχετικά με αυτές τις συνδέσεις. Σε κάθε περίπτωση, η πιθανή υπερβάλλουσα θνησιμότητα λόγω των εμβολιασμών COVID θα πρέπει να θεωρηθεί ως σήμα συναγερμού που απαιτεί στοχευμένη τεκμηρίωση και έρευνα.
Όσον αφορά την Ελλάδα και σύμφωνα με τα επίσημα στοιχεία που παρέχει ο ΟΕΔΥ, πραγματοποιήσαμε μία χρονική σύγκριση της συνολικής θνησιμότητας με τους θανάτους από/με Covid και την αναλογία Θανάτων Covid/Κρούσματα [106].
Παρατηρούμε ότι οι θάνατοι με Covid συμβαδίζουν με τη θνησιμότητα μέχρι και τον Αύγουστο του 2021. Εκείνο το μήνα παρατηρούμε μια δυσανάλογη αύξηση των θανάτων covid και της συνολικής θνησιμότητας. Η συνολική αυξάνεται δραματικά τον Σεπτέμβριο του 2021 ενώ η καμπύλη των θανάτων με covid ακολουθούν σταθερή και ήπια ανοδική αύξηση.
Συγκρίνοντας τα αριθμητικά δεδομένα, παρατηρούμε τα εξής:
Το πρώτο κρίσιμο «κύμα» φαίνεται να ξεκινάει το Νοέμβριο του 2020 (επιβεβαιώνεται και από τα στοιχεία της Euromomo) και να εξασθενεί τις πρώτες εβδομάδες του 2021. Τον Οκτώβριο του 2020 υπήρχαν 8.737 νεκροί συνολικά στην Ελλάδα και 235 νεκροί από Covid.
Το Νοέμβριο του 2020 υπήρχαν συνολικά 13.116 νεκροί και 1.780 νεκροί από Covid. Το Δεκέμβριο του 2020, η θνησιμότητα άγγιξε τους 12.686 ενώ οι νεκροί από Covid τους 2.432. Τον Ιανουάριο του 2021, οι συνολικοί νεκροί άγγιξαν τους 15.864 ενώ οι νεκροί από Covid ήταν 958. Παρατηρούμε αναλογικά ότι οι νεκροί συνολικά και οι νεκροί από Covid συμβαδίζουν, μία τέτοια όμως υπερβάλλουσα θνησιμότητα δεν μπορεί να δικαιολογηθεί στην Covid-19. Φαίνεται ότι άλλοι παράγοντες οδήγησαν στη μεγάλη αυτή αύξηση της θνησιμότητας. Ένα αντίστοιχο μοτίβο παρατηρούμε και τον Απρίλιο του 2021.
Αυτό που δεν μπορεί να αποδοθεί στην Covid είναι η υπερβάλλουσα θνησιμότητα που παρατηρήθηκε τον Αύγουστο του 2021. Ενώ τον Ιούνιο του 2021 καταγράφηκαν 9.984 συνολικά θάνατοι και 611 νεκροί από covid, τον Ιούλιο του 2021 η θνησιμότητα έφτασε τους 11.004 ενώ οι νεκροί από Covid μειώθηκαν στους 259. Η θνησιμότητα συνέχισε να αυξάνεται και τον Αύγουστο (15.110 νεκροί) ενώ οι νεκροί από Covid μόλις που άγγιξαν τους 726.
Όσον αφορά τη συσχέτιση μεταξύ εμβολιασμών και θνησιμότητας, τα στοιχεία από την Ελλάδα μας δείχνουν ότι υπάρχει έντονη χρονική συσχέτιση μεταξύ των νεκρών μετά από εμβολιασμό και της συνολικής θνησιμότητας. Να τονίσουμε ότι υπάρχει μία χρονική καθυστέρηση της πραγματικής ημερομηνίας θανάτου από την ημερομηνία αναφοράς στο σύστημα Eudravigilance. Για την εξαγωγή των αποτελεσμάτων χρησιμοποιούμε την ημερομηνία καταχώρησης στη βάση δεδομένων του ΕΜΑ. Αν υποθέσουμε ότι οι αναφορές καθυστερούν μέχρι και ένα μήνα να φτάσουν στη βάση δεδομένων του Ευρωπαϊκού Οργανισμού (Κίτρινη Κάρτα–>ΕΟΦ–>ΕΜΑ), το διορθωμένο αντίστοιχο γράφημα είναι το παρακάτω:
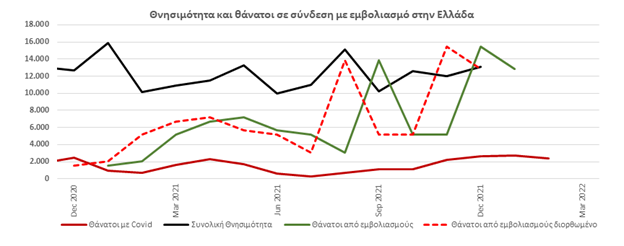
Συμπέρασμα: Το 2021, η υπερβάλλουσα θνησιμότητα εμφανίστηκε σε διαχρονική σύνδεση με τις εκστρατείες εμβολιασμού, ιδίως στις μεσαίες και νεότερες ηλικιακές ομάδες, η οποία δεν μπορεί να εξηγηθεί από την COVID. Εκτός από την έλλειψη ιατρικής περίθαλψης λόγω των μέτρων περιορισμού, η σύνδεση με τον εμβολιασμό COVID μπορεί να χαρακτηριστεί ως εύλογη και συνεπώς πιθανή.
5.8-Αποβολές και μειωμένη γονιμότητα
Η ανάλυση του αριθμού των γεννήσεων παιδιών στη Γερμανία δείχνει μείωση του ποσοστού γεννήσεων κατά 14,3% μεταξύ του πρώτου τριμήνου του 2021 και του 2022 [92]. Φαίνεται πιθανό ότι η μείωση αυτή σχετίζεται με τις εκστρατείες εμβολιασμού COVID. Ωστόσο, μια μετα-ανάλυση έδειξε ότι τουλάχιστον ο εμβολιασμός με mRNA COVID δεν σχετίζεται με αυξημένα ποσοστά αποβολής ή θνησιγένειας και ότι οι θνησιγένειες μειώθηκαν κατά 15% ως αποτέλεσμα του εμβολιασμού [93]. Ωστόσο, η μελέτη δεν κατέγραψε πρόωρες αποβολές ή αλλαγές στη γονιμότητα. Μια μελέτη για την ασφάλεια των εμβολίων που δημοσιεύθηκε στο New England Journal of Medicine φαίνεται επίσης να “αποδεικνύει” ότι ο εμβολιασμός σχετίζεται με ένα φυσιολογικό ποσοστό αποβολών. Στη μελέτη, ωστόσο, το ποσοστό αποβολών μπορεί να “αποσιωπηθεί” από το γεγονός ότι το 85% των εγκύων συμμετεχόντων δεν εμβολιάστηκαν πριν από το τρίτο τρίμηνο. Το ποσοστό αποβολών των γυναικών που έλαβαν τον εμβολιασμό COVID κατά το πρώτο τρίμηνο δεν αναφέρεται – ίσως σκόπιμα – αν και ήταν σίγουρα γνωστό στους συγγραφείς ή θα μπορούσε να υπολογιστεί από τα δεδομένα [94]. Συνεπώς, υπάρχει ανάγκη για περαιτέρω έρευνα εδώ για να αποδειχθεί ή να διαψευστεί η πιθανή βλάβη από τον εμβολιασμό COVID.
Συμπέρασμα: Η σχέση μεταξύ της μειωμένης γονιμότητας και του ρυθμού γεννήσεων φαίνεται πιθανή, αλλά πρέπει να αποδειχθεί ή να διαψευστεί με περαιτέρω έρευνα.
6-Σχέση οφέλους-κινδύνου των εμβολιασμών COVID
Η δευτερογενής ανάλυση των μελετών καταχώρισης των εμβολίων mRNA υποδηλώνει αρνητική σχέση οφέλους-κινδύνου. Είναι πιθανόν ο κίνδυνος σοβαρών (SAE) και ειδικών (AESI) παρενεργειών να είναι υπερδιπλάσιος (Spikevax®) ή ακόμη και πενταπλάσιος (Comirnaty®) από την πιθανότητα αποφυγής νοσηλείας που σχετίζεται με την COVID μέσω του εμβολιασμού. Δεν υπάρχουν ακόμη έγκυρα δεδομένα ανά ηλικία και δεδομένα που να λαμβάνουν υπόψη τη συννοσηρότητα. Μέχρι σήμερα, δεν υπάρχει ούτε ένα αξιόπιστο στοιχείο που να αποδεικνύει ότι ο εμβολιασμός μειώνει την ολική θνησιμότητα.
Λαμβάνοντας υπόψη την έλλειψη δεδομένων σχετικά με τα αποτελέσματα που αφορούν τους ασθενείς, την έλλειψη μακροπρόθεσμων δεδομένων και την έλλειψη δεδομένων σχετικά με τα αποτελέσματα του εμβολιασμού σε επιμέρους ομάδες ηλικίας και κινδύνου, πρέπει να υποτεθεί ότι το όφελος του εμβολιασμού που αντισταθμίζει την πιθανή βλάβη δεν είναι δεδομένο για τους περισσότερους ανθρώπους. Αυτό ισχύει ιδιαίτερα για τα παιδιά και τους νέους, και με μεγάλη πιθανότητα και για τα υγιή άτομα μέσης και μεγαλύτερης ηλικίας.
Δεν έχει επίσης αποδειχθεί μέχρι στιγμής ότι υπάρχει όφελος από την έμμεση προστασία των ατόμων που διατρέχουν κίνδυνο μέσω της υψηλότερης δυνατής εμβολιαστικής κάλυψης του πληθυσμού, η οποία θα δικαιολογούσε τον κίνδυνο μέσω του εμβολιασμού νέων και υγιών ατόμων. Επίσης, δεν υπάρχει καμία απόδειξη ότι ο μαζικός εμβολιασμός έχει μόνιμο αντίκτυπο στα επιδημιολογικά γεγονότα στο σύνολό τους. Αντιθέτως, μόνο μετά την εισαγωγή του εμβολιασμού σημειώθηκαν οι μεγάλες μαζικές επιδημίες της COVID από τις μεταλλάξεις δέλτα και όμικρον.
Συμπέρασμα: Για τα παιδιά, τους νέους και τους υγιείς ανθρώπους, καθώς και για τους ήδη νοσήσαντες, η βλάβη του εμβολιασμού COVID αντισταθμίζει το πιθανό όφελος. Αυτή η αρνητική σχέση κινδύνου-οφέλους μπορεί να αποδειχθεί με πολυάριθμες μελέτες. Το κατά πόσον οι ηλικιωμένοι με προϋπάρχουσες παθήσεις ωφελούνται από τον εμβολιασμό είναι άγνωστο, καθώς οι διαθέσιμες μελέτες έχουν πολλά μεθοδολογικά σφάλματα ή δεν ήταν δυνατή ή δεν πραγματοποιήθηκε ανάλυση υποομάδων του πληθυσμού κινδύνου.
7. Ενδείξεις εμβολιασμών COVID με δυνητικά ευνοϊκή σχέση κινδύνου-οφέλους
Ο κίνδυνος για σοβαρή εξέλιξη της COVID και για θάνατο από COVID αφορά κυρίως ηλικιωμένα άτομα με συνοδά νοσήματα. Η ηλικία, οι συνοδές νόσοι και ο κίνδυνος λοίμωξης πρέπει να περιλαμβάνονται στον υπολογισμό του κινδύνου. Ένας τέτοιος υπολογισμός είναι δυνατός, για παράδειγμα, με τον υπολογιστή κινδύνου QCOVID (https://qcovid.org/Calculation/Unvaccinated ), ο οποίος επικυρώθηκε σε μια μεγάλη συλλογική ομάδα [95]. Μόνο από έναν κίνδυνο θανάτου COVID σημαντικά μεγαλύτερο από 1/10.000 το όφελος του εμβολιασμού υπερβαίνει τον πιθανό κίνδυνο θανάτου από τον εμβολιασμό. Αντίστοιχος υπολογιστής κινδύνου υπάρχει και στα Ελληνικά (https://www.eyewideopen.org/calc/vacc_risk.html )Πρέπει επίσης να ληφθεί υπόψη ότι η επικύρωση του υπολογιστή πραγματοποιήθηκε στην μετάλλαξη άλφα και ότι ο κίνδυνος από την μετάλλαξη όμικρον είναι πιθανώς σημαντικά χαμηλότερος. Πρέπει επίσης να ληφθεί υπόψη ότι η απόδειξη του οφέλους δεν υποστηρίζεται από μελέτες υψηλής ποιότητας. Επιπλέον, ο ενδιαφερόμενος πρέπει φυσικά να ενημερωθεί για τους μακροπρόθεσμους κινδύνους που δεν έχουν ακόμη διερευνηθεί και για την παρατηρούμενη επί του παρόντος ελλιπή αναφορά παρενεργειών, οι οποίες δεν θα μπορούσαν να συμπεριληφθούν στον παρόντα υπολογισμό λόγω της έλλειψης μακροπρόθεσμων μελετών και αναφορών παρενεργειών.
Λόγω της έλλειψης στείρας ανοσίας και του ομοίως υψηλού ιικού φορτίου σε μολυσμένα εμβολιασμένα άτομα που έχει αποδειχθεί σε μελέτες, η προστασία των ευάλωτων ανεμβολίαστων ή μη εμβολιασμένων ατόμων δεν αποτελεί ένδειξη για τον εμβολιασμό COVID, καθώς δεν προστατεύει από τη μόλυνση ούτε μπορεί να δημιουργήσει ανοσία αγέλης.
Συμπέρασμα: Ένδειξη για τον εμβολιασμό κατά της COVID υπάρχει στην καλύτερη περίπτωση σε περίπτωση υψηλού προσωπικού κινδύνου σοβαρής νόσου COVID ή θανάτου από COVID. Ο εμβολιασμός COVID δεν ενδείκνυται ούτε για άτομα με χαμηλό κίνδυνο COVID ούτε για την προστασία άλλων ατόμων.
8. Αντενδείξεις για τον εμβολιασμό COVID λόγω πιθανής αρνητικής σχέσης κινδύνου-οφέλους
Εκτός από την έλλειψη ενδείξεων σε υγιή και νεαρά άτομα, οι εμβολιασμοί COVID αντενδείκνυνται σε ορισμένα άτομα λόγω έλλειψης δεδομένων και ιδιαίτερα υψηλού κινδύνου σοβαρών παρενεργειών. Αυτή η ομάδα ατόμων περιλαμβάνει ιδίως εκείνους για τους οποίους υπάρχει η υποψία για σοβαρές παρενέργειες σύμφωνα με το σχέδιο διαχείρισης κινδύνου του κατασκευαστή ή για τους οποίους δεν υπάρχουν επαρκή δεδομένα ασφάλειας:
- Αλλεργική διάγνωση, ιστορικό αλλεργικών αντιδράσεων σε εμβόλια ή συστατικά του εμβολίου
COVID, πολυαλλεργικό σύνδρομο, γύρη, τροφική αλλεργία.
- Αυτοάνοσα νοσήματα, π.χ. ψωρίαση, νευροδερματίτιδα, ερυθηματώδης λύκος, ρευματοειδή νοσήματα, θυρεοειδίτιδα Hashimoto, νόσος του Crohn, ελκώδης κολίτιδα, βολβοειδές έκζεμα, πεμφιγοειδές.
- Διαταραχές πήξης, π.χ. τάση αιμορραγίας, θρομβοφιλία, παράγοντας V Leiden, θρομβώσεις ή εμβολές στο ιστορικό, λήψη αντιπηκτικών φαρμάκων ή αναστολέων της συσσώρευσης των αιμοπεταλίων.
- Ιστορικό αγγειίτιδας (φλεγμονή των αιμοφόρων αγγείων)
- Ιστορικό καρκίνου ή τρέχουσα θεραπεία για καρκίνο
- Ασθένειες του λεμφικού συστήματος, λεμφοίδημα, λευχαιμία, λέμφωμα
- Καρδιακή νόσος, π.χ. ιστορικό μυοκαρδίτιδας ή περικαρδίτιδας, στεφανιαία νόσος.
- Προϋπάρχουσες νευρολογικές παθήσεις, π.χ. πολυνευροπάθεια, επιληψία, νόσος του Πάρκινσον, σκλήρυνση κατά πλάκας, αμυοτροφική πλευρική σκλήρυνση (ALS).
- Προϋπάρχουσες λοιμώξεις με κίνδυνο υποτροπής, π.χ. φυματίωση, νόσος του Lyme, έρπητας ζωστήρας (ιοί έρπητα), ιός Epstein Barr, ηπατίτιδα Β, ηπατίτιδα C.
- Εμμηνορροϊκές κράμπες, αποβολές στο παρελθόν
- Έγκυες γυναίκες και γυναίκες που θέλουν να μείνουν έγκυες
- Αθλητές υψηλών επιδόσεων, επαγγελματίες ποδοσφαιριστές και καλά προπονημένοι άνδρες καθώς και μαραθωνοδρόμοι, ακόμη και χωρίς προϋπάρχουσες παθήσεις.
- Άνθρωποι που απορρίπτουν δυνητικά μέτρα γονιδιακής τροποποίησης για τον εαυτό τους για ηθικούς λόγους
- Άνθρωποι που απορρίπτουν δυνητικά μέτρα γονιδιακής τροποποίησης για τον εαυτό τους για θρησκευτικούς λόγους
Συμπέρασμα: Με την παρουσία ασθενειών ή παραγόντων κινδύνου που αντιστοιχούν στο φάσμα της AESI, καθώς και με την παρουσία ασθενειών ή καταστάσεων για τις οποίες δεν υπάρχουν επαρκή δεδομένα ασφάλειας, ο εμβολιασμός με COVID δεν θα πρέπει να πραγματοποιείται έως ότου αποδειχθούν τα κατάλληλα δεδομένα ασφάλειας.
9- Αξιολόγηση των διαθέσιμων στοιχείων των μελετών σύμφωνα με το GRADE
Προκειμένου να μεταβούμε από τα διαθέσιμα στοιχεία μελετών σε κλινικές αποφάσεις, είναι απαραίτητο να αξιολογηθεί η ποιότητα των στοιχείων και να αναφερθεί η ισχύς των ιατρικών συστάσεων. Για το σκοπό αυτό, μια διεθνής ομάδα εργασίας ανέπτυξε το σύστημα GRADE (Grading of Recommendations Assessment, Development and Evaluation) [96]. Σύμφωνα με την GRADE, τα στοιχεία των μελετών χωρίζονται σε τέσσερα επίπεδα (βλ. Πίνακα 3) και οι συστάσεις που προκύπτουν από τα στοιχεία κατατάσσονται ως ισχυρές ή ασθενείς.
| Ποιότητα των αποδεικτικών στοιχείων | Σημασία | Υποκείμενες μελέτες |
| Υψηλή | Είναι πολύ απίθανο η μελλοντική έρευνα να αλλάξει την εμπιστοσύνη μας στο μετρούμενο αποτέλεσμα. | Τυχαιοποιημένες ελεγχόμενες δοκιμές (RCT), μετα-αναλύσεις από RCTs |
| Μέτρια | Είναι πιθανό ότι η μελλοντική έρευνα θα αλλάξει την εμπιστοσύνη μας στο μετρούμενο αποτέλεσμα | Τυχαιοποιημένες ελεγχόμενες μελέτες με μεθοδολογικά σφάλματα και κίνδυνο μεροληψίας (ασυνέπεια αποτελεσμάτων, έμμεσες ενδείξεις κ.λπ. μορφές μεροληψίας) |
| Χαμηλή | Είναι πολύ πιθανό ότι η μελλοντική έρευνα θα αλλάξει την εμπιστοσύνη μας στο μετρούμενο αποτέλεσμα | Μελέτες κοόρτης και ελέγχου περιπτώσεων |
| Πολύ χαμηλή | Η εκτίμηση του αποτελέσματος υπόκειται σε μεγάλη αβεβαιότητα | Μελέτες κοόρτης και ελέγχου περιπτώσεων με μεθοδολογικές αδυναμίες, σειρές περιπτώσεων, μελέτες συσχέτισης |
Μεγάλες επιδράσεις, σαφής εξάρτηση της επίδρασης από τη δόση και εύλογα στοιχεία ότι η υπάρχουσα μεροληψία στην καλύτερη περίπτωση μειώνει την επίδραση μπορούν να οδηγήσουν σε “αναβάθμιση”, μεθοδολογικές αδυναμίες και μεροληψία στην “Υποβάθμιση“.
Οι ισχυρές αποφάσεις βασίζονται σε ένα σαφές όφελος από την παρέμβαση που έχει αποδειχθεί με υψηλά αποδεικτικά στοιχεία. Αδύναμες συστάσεις γίνονται όταν δεν είναι σαφές εάν τα οφέλη υπερτερούν των κινδύνων.
Μεταφερόμενοι στον εμβολιασμό COVID, μπορεί να δηλωθεί ότι τα διαθέσιμα στοιχεία μελετών για την πρόληψη σοβαρών περιπτώσεων και θανάτων μέσω του εμβολιασμού στηρίζονται αποκλειστικά σε μεθοδολογικά αμφισβητήσιμες μελέτες κοόρτης και μελέτες ελέγχου περιπτώσεων που χαρακτηρίζονται από υψηλή πιθανότητα μεροληψίας και μπορούν συνεπώς να καταταγούν στο χαμηλότερο επίπεδο τεκμηρίωσης σύμφωνα με την GRADE. Δεδομένου ότι δεν υπάρχει σαφής αντιστάθμιση των ωφελειών έναντι των κινδύνων, μπορεί να δοθεί μόνο μια ασθενής σύσταση για εμβολιασμό, ακόμη και για άτομα με υψηλό κίνδυνο σοβαρής νόσου COVID.
10-Ενημερωμένη και συμμετοχική λήψη αποφάσεων για τον εμβολιασμό με βάση την τεκμηρίωση
Εκτός από τον πυλώνα των διαθέσιμων στοιχείων μελετών, η ιατρική που βασίζεται σε αποδείξεις περιλαμβάνει τους εξίσου σημαντικούς πυλώνες της “ιατρικής, κλινικής εμπειρογνωμοσύνης” και των “αξιών των ασθενών” [97].
Ο πυλώνας της “ιατρικής, κλινικής εμπειρογνωμοσύνης” είναι απολύτως απαραίτητος για την τεκμηριωμένη ιατρική δράση, διότι τα στοιχεία των μελετών (ο πρώτος πυλώνας της τεκμηριωμένης ιατρικής) λαμβάνονται πάντα από πληθυσμούς ασθενών ή υποκειμένων και οι κατευθυντήριες γραμμές είναι επομένως προσανατολισμένες σε πληθυσμούς και όχι σε μεμονωμένους ασθενείς. Η δυνατότητα μεταφοράς των στοιχείων της μελέτης σε μεμονωμένους ασθενείς δεν είναι λειτουργεί ποτέ 100% και απαιτεί την προσεκτική αξιολόγηση ενός έμπειρου ιατρού. Για το λόγο αυτό, οι ιατρικές κατευθυντήριες γραμμές δεν είναι νομικά δεσμευτικές για τη θεραπεία μεμονωμένων ασθενών.
Ο τρίτος πυλώνας, οι αξίες του ασθενούς, είναι εξίσου απαραίτητος με τους δύο πρώτους πυλώνες, διότι κάθε άνθρωπος δικαιούται να έχει τον τελικό λόγο για το ποια ιατρικά μέτρα θα εφαρμοστούν στο σώμα, την ψυχή και το πνεύμα του. Για το σκοπό αυτό υπάρχει, μεταξύ άλλων, η προσωπική διαθήκη ζωής, η οποία θέτει τις ατομικές αποφάσεις του ασθενούς πάνω απ’ όλα, πέρα από κάθε επιστήμη.
Όλα αυτά πρέπει φυσικά να ισχύουν και για τους εμβολιασμούς COVID. Λαμβάνοντας υπόψη την έλλειψη αποτελεσματικότητας των εμβολιασμών όσον αφορά την προστασία από τη μόλυνση και τη νόσο, τη μετάδοση της μόλυνσης και την επίτευξη ανοσίας αγέλης, η μόνη πιθανή ένδειξη που απομένει είναι η φαινομενικά πιθανή προστασία του εμβολιασμένου ατόμου από μια σοβαρή εξέλιξη της COVID. Προκειμένου να καταστεί δυνατή η λήψη τεκμηριωμένης, συμμετοχικής απόφασης από τον ασθενή, πρέπει να παρέχονται ολοκληρωμένες πληροφορίες σχετικά με τους πιθανούς κινδύνους του εμβολιασμού, λαμβάνοντας υπόψη τόσο το γνωστό προφίλ παρενεργειών του εμβολίου όσο και τον προφίλ κινδύνου του ατόμου που πρόκειται να εμβολιαστεί. Επιπλέον, πρέπει να επισημανθεί η πιθανότητα περαιτέρω παρενεργειών που δεν έχουν ακόμη αποδειχθεί με βεβαιότητα, η έλλειψη δεδομένων μακροπρόθεσμης ασφάλειας και η υπό όρους έγκριση των εμβολίων.
11-Προοπτικές
Μόνο κλινικές μελέτες που διερεύνησαν αποτελέσματα σχετικά με τον ασθενή συμπεριλήφθηκαν στην παρούσα περίληψη στοιχείων. Παθοφυσιολογικές εκτιμήσεις, εικασίες και μεμονωμένες αναφορές περιπτώσεων σκόπιμα δεν συμπεριλήφθηκαν. Ωστόσο, θα πρέπει να επισημανθεί ρητά στο τέλος αυτής της ανάλυσης στοιχείων ότι οι πιθανές μελλοντικές βλάβες από τους εμβολιασμούς COVID δεν θα μπορούσαν καν να καταγραφούν ακόμη λόγω της βραχύτητας της περιόδου παρατήρησης και λόγω της αποτυχίας διεξαγωγής μελετών φάσης IV και μεθόδων φαρμακοεπαγρύπνησης. Για παράδειγμα, εικάζεται τόσο η καρκινογόνος όσο και η προφλεγμονώδης επίδραση των λιπιδικών νανοσωματιδίων που μεταφέρουν το τροποποιημένο mRNA του εμβολίου στο κύτταρο [98,99].
Μια φλεγμονώδης αντίδραση στο ίδιο το τροποποιημένο mRNA καθώς και περαιτέρω βλάβες του ανοσοποιητικού συστήματος φαίνονται επίσης πιθανές. Επομένως, θα πρέπει να αναλυθεί πολύ προσεκτικά αν θα υπάρξει αύξηση του καρκίνου και των χρόνιων φλεγμονωδών νοσημάτων, καθώς και των άτυπων λοιμωδών νοσημάτων, συμπεριλαμβανομένης της επανενεργοποίησης λανθάνουσας λοίμωξης στα εμβολιασμένα άτομα, δεδομένου ότι δεν θα είναι πιθανόν να διακρίνεται άμεση χρονική σύνδεση μεταξύ εμβολιασμού και εκδήλωσης ασθενειών.
Εκτός από την πιθανή ανοσοκαταστολή (V-AIDS) μέσω των επαναλαμβανόμενων εμβολιασμών, δεν μπορεί να αποκλειστεί η λεγόμενη αντισωματοεξαρτώμενη ενίσχυση (Antibody-Dependent Enhancement-ADE) με ιδιαίτερα σοβαρές εξελίξεις της νόσου [100]. Συζητείται επίσης μια πιθανή ευνοϊκή επίδραση στην ανάπτυξη και επιδείνωση αυτοάνοσων νοσημάτων [101].
Η παρούσα περίληψη των στοιχείων δεν μπορεί να παράσχει μια ολοκληρωμένη περιγραφή αυτών των πιθανών παρενεργειών και όψιμων επιδράσεων. Ωστόσο, επισημαίνεται ρητά ότι εδώ είναι απολύτως απαραίτητες μελέτες υψηλής ποιότητας προκειμένου να αποδειχθεί η μακροπρόθεσμη ασφάλεια των εμβολίων όσον αφορά αυτές τις παθοφυσιολογικά πιθανές επιδράσεις.
12-Βιβλιογραφία
- Johns Hopkins University Corona Virus Resource Center. COVID-19 Dashboard by the Center for Science and Engineering (CSSE) at Johns Hopkins University (JHU) [Internet]. 2022 [zitiert 2022 Mai 30];Available from: https://coronavirus.jhu.edu/map.html
- Statista [Διαδίκτυο]. 2022 https://www.statista.com/statistics/1219343/covid19-vaccine-doses-distributed-in-europe-by-manufacturer/
- Davies MA, Kassanjee R, Rousseau P, Morden E, Johnson L, Solomon W, et al. Outcomes of laboratoryconfirmed SARS-CoV-2 infection in the Omicron-driven fourth wave compared with previous waves στην επαρχία του Δυτικού Ακρωτηρίου, Νότια Αφρική [Internet]. Infectious Diseases (except HIV/AIDS); 2022 [cited 2022 May 30]. Available from: http://medrxiv.org/lookup/doi/10.1101/2022.01.12.22269148
- BKK ProVita. Παρενέργειες του εμβολιασμού Corona [Internet]. 2022 [cited 2022 March 11]. Διαθέσιμο από: https://web.archive.org/web/20220225182653/https://bkk-provita.de/wpcontent/uploads/2022/02/Annex-side-effects-Corona-vaccination.pdf
- Mi YN, Huang TT, Zhang JX, Qin Q, Gong YX, Liu SY, u. a. Estimating the instant case fatality rate of COVID-19 in China. Int J Infect Dis 2020;97:1–6.
- Streeck H, Schulte B, Kuemmerer B, Richter E, Hoeller T, Fuhrmann C, et al. Ποσοστό θνησιμότητας της λοίμωξης SARS-CoV-2 σε μια γερμανική κοινότητα με ένα γεγονός υπερδιάδοσης [Internet]. Infectious Diseases (except HIV/AIDS); 2020 [ανακτήθηκε 2020 Aug 19]. Available from: http://medrxiv.org/lookup/doi/10.1101/2020.05.04.20090076
- Ioannidis JPA. Reconciling estimates of global spread and infection fatality rates of COVID-19: An overview of systematic evaluations. Eur J Clin Invest 2021;51:e13554.
- Centers for Disease Control and Prevention. Disease Burden of Flu [Internet]. [cited 2022 Mai 31]; Διαθέσιμο από: https://www.cdc.gov/flu/about/burden/index.html
- Onder G, Rezza G, Brusaferro S. Case-Fatality Rate and Characteristics of Patients Dying in Relation to COVID-19 in Italy. JAMA 2020;323:1775–6.
- Wu Z, McGoogan JM. Characteristics of and Important Lessons From the Coronavirus Disease 2019 (COVID-19) Outbreak in China: Summary of a Report of 72 314 Cases From the Chinese Center for Disease Control and Prevention. JAMA 2020;323:1239–42.
- Wolter N, Jassat W, Walaza S, Welch R, Moultrie H, Groome M, u. a. Early assessment of the clinical severity of the SARS-CoV-2 omicron variant in South Africa: a data linkage study. The Lancet 2022;399:437–46.
- Oran DP, Topol EJ. The Proportion of SARS-CoV-2 Infections That Are Asymptomatic: A Systematic Review. Ann Intern Med 2021;174:655–62
- Polack FP, Thomas SJ, Kitchin N, Absalon J, Gurtman A, Lockhart S, u. a. Safety and Efficacy of the BNT162b2 mRNA Covid-19 Vaccine. N Engl J Med 2020;383:2603–15.
- Baden LR, El Sahly HM, Essink B, Kotloff K, Frey S, Novak R, u. a. Efficacy and Safety of the mRNA1273 SARS-CoV-2 Vaccine. N Engl J Med 2021;384:403–16.
- Voysey M, Clemens SAC, Madhi SA, Weckx LY, Folegatti PM, Aley PK, u. a. Safety and efficacy of the ChAdOx1 nCoV-19 vaccine (AZD1222) against SARS-CoV-2: an interim analysis of four randomised controlled trials in Brazil, South Africa, and the UK. Lancet 2021;397:99–111.
- Sadoff J, Gray G, Vandebosch A, Cárdenas V, Shukarev G, Grinsztejn B, u. a. Safety and Efficacy of Single-Dose Ad26.COV2.S Vaccine against Covid-19. N Engl J Med 2021;384:2187–201
- Dunkle LM, Kotloff KL, Gay CL, Áñez G, Adelglass JM, Barrat Hernández AQ, u. a. Efficacy and Safety of NVX-CoV2373 in Adults in the United States and Mexico. N Engl J Med 2022;386:531–43
- Heath PT, Galiza EP, Baxter DN, Boffito M, Browne D, Burns F, u. a. Safety and Efficacy of NVXCoV2373 Covid-19 Vaccine. N Engl J Med 2021;385:1172–83.
- Συνεδρίαση της συμβουλευτικής επιτροπής εμβολίων και συναφών βιολογικών προϊόντων. Έγγραφο ενημέρωσης του FDA – Εμβόλιο Pfizer-BioNTech COVID-19 [Internet]. [cited 2022 May 31]. Διαθέσιμο από: https://www.fda.gov/media/144245/download
- Pfizer. A PHASE 1/2/3, PLACEBO-CONTROLLED, RANDOMIZED, OBSERVER-BLIND, DOSE-FINDING STUDY TO EVALUATE THE SAFETY, TOLERABILITY, IMMUNOGENICITY, AND EFFICACY OF SARSCOV-2 RNA VACCINE CANDIDATES AGAINST COVID-19 IN HEALTHY INDIVIDUALS [Internet]. 2020. Available from: https://cdn.pfizer.com/pfizercom/2020-11/C4591001_Clinical_Protocol_Nov2020.pdf
- Moderna. A Phase 3, Randomized, Stratified, Observer-Blind, Placebo-Controlled Study to Evaluate the Efficacy, Safety, and Immunogenicity of mRNA-1273 SARS-CoV-2 Vaccine in Adults Aged 18 Years and Older [Internet]. 2020 [cited 2022 June 1];Διαθέσιμο από: https://covid19crc.org/wpcontent/uploads/2020/09/mRNA-1273-P301-Protocol-2020.pdf
- Thomas SJ, Moreira ED, Kitchin N, Absalon J, Gurtman A, Lockhart S, u. a. Safety and Efficacy of the BNT162b2 mRNA Covid-19 Vaccine through 6 Months. N Engl J Med 2021;385:1761–73.
- Benn CS, Schaltz-Buchholzer F, Nielsen S, Netea MG, Aaby P. Randomised Clinical Trials of COVID-19 Vaccines: Do Adenovirus-Vector Vaccines Have Beneficial Non-Specific Effects? SSRN Journal [Internet] 2022 [cited 2022 June 8]. Διαθέσιμο από: https://www.ssrn.com/abstract=4072489
- Dagan N, Barda N, Kepten E, Miron O, Perchik S, Katz MA, u. a. BNT162b2 mRNA Covid-19 Vaccine in a Nationwide Mass Vaccination Setting. N Engl J Med 2021;384:1412–23.
- Florea A, Sy LS, Luo Y, Qian L, Bruxvoort KJ, Ackerson BK, u. a. Durability of mRNA-1273 against COVID-19 in the time of Delta: Interim results from an observational cohort study. PLoS ONE 2022;17:e0267824.
- Vasileiou E, Simpson CR, Shi T, Kerr S, Agrawal U, Akbari A, u. a. Interim findings from first-dose mass COVID-19 vaccination roll-out and COVID-19 hospital admissions in Scotland: a national prospective cohort study. Lancet 2021;397:1646–57
- Haas EJ, Angulo FJ, McLaughlin JM, Anis E, Singer SR, Khan F, u. a. Impact and effectiveness of mRNA BNT162b2 vaccine against SARS-CoV-2 infections and COVID-19 cases, hospitalisations and deaths following a nationwide vaccination campaign in Israel: an observational study using national surveillance data. Lancet 2021;397:1819–29.
- Barda N, Dagan N, Cohen C, Hernán MA, Lipsitch M, Kohane IS, u. a. Effectiveness of a third dose of the BNT162b2 mRNA COVID-19 vaccine for preventing severe outcomes in Israel: an observational study. The Lancet 2021;398:2093–100
- Bar-On YM, Goldberg Y, Mandel M, Bodenheimer O, Freedman L, Kalkstein N, u. a. Protection of BNT162b2 Vaccine Booster against Covid-19 in Israel. N Engl J Med 2021;385:1393–400
- Russo AG, Murtas R, Tunesi S, Decarli A, Bergamaschi W. Booster e distanza dall’ultima dose vaccinale anti-COVID-19: la valutazione epidemiologica continua per orientare le scelte di sanità pubblica. E&P 2022;46:1–13.
- Nordström P, Ballin M, Nordström A. Risk of infection, hospitalisation, and death up to 9 months after a second dose of COVID-19 vaccine: a retrospective, total population cohort study in Sweden. Lancet 2022;399:814–23
- Goldberg Y, Mandel M, Bar-On YM, Bodenheimer O, Freedman L, Haas EJ, u. a. Waning Immunity after the BNT162b2 Vaccine in Israel. N Engl J Med 2021;385:e85
- Tartof SY, Slezak JM, Fischer H, Hong V, Ackerson BK, Ranasinghe ON, u. a. Effectiveness of mRNA BNT162b2 COVID-19 vaccine up to 6 months in a large integrated health system in the USA: a retrospective cohort study. Lancet 2021;398:1407–16.
- Ramesh S, Govindarajulu M, Parise RS, Neel L, Shankar T, Patel S, u. a. Emerging SARS-CoV-2Variants: A Review of Its Mutations, Its Implications and Vaccine Efficacy. Vaccines 2021;9:1195
- European Centre for Disease Prevention and Control. SARS-CoV-2 variants of concern as of 25 May 2022 [Internet]. 2022 [cited 2022 Juni 9];Available from: https://www.ecdc.europa.eu/en/covid-19/variants-concern
- Hayawi K, Shahriar S, Serhani MA, Alashwal H, Masud MM. Vaccine versus Variants (3Vs): Are the COVID-19 Vaccines Effective against the Variants? A Systematic Review. Vaccines 2021;9:1305
- Lopez Bernal J, Andrews N, Gower C, Gallagher E, Simmons R, Thelwall S, u. a. Effectiveness of Covid- 9 Vaccines against the B.1.617.2 (Delta) Variant. N Engl J Med 2021;385:585–94.
- Subramanian SV, Kumar A. Increases in COVID-19 are unrelated to levels of vaccination across 68 countries and 2947 counties in the United States. Eur J Epidemiol 2021;36:1237–40.
- Andrews N, Stowe J, Kirsebom F, Toffa S, Rickeard T, Gallagher E, u. a. Covid-19 Vaccine Effectiveness against the Omicron (B.1.1.529) Variant. N Engl J Med 2022;386:1532–46
- Frenck RW, Klein NP, Kitchin N, Gurtman A, Absalon J, Lockhart S, u. a. Safety, Immunogenicity, and Efficacy of the BNT162b2 Covid-19 Vaccine in Adolescents. N Engl J Med 2021;385:239–50.
- Creech CB, Anderson E, Berthaud V, Yildirim I, Atz AM, Melendez Baez I, u. a. Evaluation of mRNA-1273 Covid-19 Vaccine in Children 6 to 11 Years of Age. N Engl J Med 2022;386:2011–23.
- Ali K, Berman G, Zhou H, Deng W, Faughnan V, Coronado-Voges M, u. a. Evaluation of mRNA-1273 SARS-CoV-2 Vaccine in Adolescents. N Engl J Med 2021;385:2241–51.
- Walter EB, Talaat KR, Sabharwal C, Gurtman A, Lockhart S, Paulsen GC, u. a. Evaluation of the BNT162b2 Covid-19 Vaccine in Children 5 to 11 Years of Age. N Engl J Med 2022;386:35–46.
- Glatman-Freedman A, Hershkovitz Y, Kaufman Z, Dichtiar R, Keinan-Boker L, Bromberg M. Effectiveness of BNT162b2 Vaccine in Adolescents during Outbreak of SARS-CoV-2 Delta Variant Infection, Israel, 2021. Emerg. Infect. Dis. 2021;27:2919–22.
- Price AM, Olson SM, Newhams MM, Halasa NB, Boom JA, Sahni LC, u. a. BNT162b2 Protection against the Omicron Variant in Children and Adolescents. N Engl J Med 2022;386:1899–909.
- Olson SM, Newhams MM, Halasa NB, Price AM, Boom JA, Sahni LC, u. a. Effectiveness of BNT162b2 Vaccine against Critical Covid-19 in Adolescents. N Engl J Med 2022;386:713–23.
- Olson SM, Newhams MM, Halasa NB, Price AM, Boom JA, Sahni LC, u. a. Effectiveness of Pfizer-BioNTech mRNA Vaccination Against COVID-19 Hospitalization Among Persons Aged 12–18 Years —United States, June–September 2021. MMWR Morb. Mortal. Wkly. Rep. 2021;70:1483–8.
- Dorabawila V, Hoefer D, Bauer UE, Bassett MT, Lutterloh E, Rosenberg ES. Effectiveness of the BNT162b2 vaccine among children 5-11 and 12-17 years in New York after the Emergence of the Omicron Variant [Internet]. Epidemiology; 2022 [cited 2022 Juni 23]. Available from: http://medrxiv.org/lookup/doi/10.1101/2022.02.25.22271454
- Abu-Raddad LJ, Chemaitelly H, Bertollini R. Severity of SARS-CoV-2 Reinfections as Compared with Primary Infections. N Engl J Med 2021;385:2487–9.
- León TM, Dorabawila V, Nelson L, Lutterloh E, Bauer UE, Backenson B, u. a. COVID-19 Cases and Hospitalizations by COVID-19 Vaccination Status and Previous COVID-19 Diagnosis — California and New York, May–November 2021. MMWR Morb. Mortal. Wkly. Rep. 2022;71:125–31.
- Al-Aly Z, Bowe B, Xie Y. Long COVID after breakthrough SARS-CoV-2 infection. Nat Med [Internet] 2022 [cited 2022 Juni 14];Available from: https://www.nature.com/articles/s41591-022-01840-0
- Ayoubkhani D, Bermingham C, Pouwels KB, Glickman M, Nafilyan V, Zaccardi F, u. a. Trajectory of long covid symptoms after covid-19 vaccination: community based cohort study. BMJ 2022;e069676.
- Riemersma KK, Grogan BE, Kita-Yarbro A, Halfmann PJ, Segaloff HE, Kocharian A, u. a. Shedding of Infectious SARS-CoV-2 Despite Vaccination [Internet]. Infectious Diseases (except HIV/AIDS); 2021 [zitiert 2022 Juni 9]. Available from: http://medrxiv.org/lookup/doi/10.1101/2021.07.31.21261387
- Singanayagam A, Hakki S, Dunning J, Madon KJ, Crone MA, Koycheva A, u. a. Communitytransmission and viral load kinetics of the SARS-CoV-2 delta (B.1.617.2) variant in vaccinated and unvaccinated individuals in the UK: a prospective, longitudinal, cohort study. The Lancet Infectious Diseases 2022;22:183–95.
- Eyre DW, Taylor D, Purver M, Chapman D, Fowler T, Pouwels KB, u. a. Effect of Covid-19 Vaccination on Transmission of Alpha and Delta Variants. N Engl J Med 2022;386:744–56.
- Lyngse FP, Mortensen LH, Denwood MJ, Christiansen LE, Møller CH, Skov RL, u. a. SARS-CoV-2 Omicron VOC Transmission in Danish Households [Internet]. Infectious Diseases (except HIV/AIDS). 2021 [cited 2022 Juni 9]. Available from: http://medrxiv.org/lookup/doi/10.1101/2021.12.27.21268278
- European Medicines Agency. Conditional Marketing Authorization [Internet]. 2020 [cited 2022 Juni 10];Available from: https://www.ema.europa.eu/en/human-regulatory/marketingauthorisation/conditional-marketing-authorisation
- Fraiman J, Erviti J, Jones J, Greenland S, Whelan P, Kaplan R, u. a. Serious Adverse Events of Special Interest Following mRNA Vaccination in Randomized Trials. JVAC-D-22-01206 [Internet] 2022 [zitiert 2022 Juni 22];Available from: https://ssrn.com/abstract=4125239
- Demicheli V, Jefferson T, Ferroni E, Rivetti A, Di Pietrantonj C. Vaccines for preventing influenza in healthy adults. Cochrane Database of Systematic Reviews [Internet] 2018 [zitiert 2022 Juni 13];2020. Available from: http://doi.wiley.com/10.1002/14651858.CD001269.pub6
- Barda N, Dagan N, Ben-Shlomo Y, Kepten E, Waxman J, Ohana R, u. a. Safety of the BNT162b2 mRNA Covid-19 Vaccine in a Nationwide Setting. N Engl J Med 2021;385:1078–90.
- Pfizer. Comirnaty Risk Management Plan 5.0 [Internet]. 2022 [zitiert 2022 Juni 14];Available from: https://www.ema.europa.eu/en/documents/rmp-summary/comirnaty-epar-risk-managementplan_en.pdf
- Janssen. European Union Risk Management Plan VAC31518 (Ad26.COV2.S) [Internet]. 2022 [zitiert 2022 Juni 14];Available from: https://www.ema.europa.eu/en/documents/rmp-summary/covid-19-vaccine-janssen-epar-risk-management-plan_en.pdf
- Novavax. EU RISK MANAGEMENT PLAN NUVAXOVID (COVID-19 VACCINE (RECOMBINANT, ADJUVANTED)) [Internet]. 2021 [zitiert 2022 Juni 14];Available from: https://www.ema.europa.eu/en/documents/rmp-summary/nuvaxovid-epar-risk-managementplan_en.pdf
- Moderna. EU Risk Management Plan for Spikevax (COVID-19mRNA vaccine) [Internet]. 2022 [zitiert 2022 Juni 14];Available from: https://www.ema.europa.eu/en/documents/rmp-summary/spikevaxpreviously-covid-19-vaccine-moderna-epar-risk-management-plan_en.pdf
- AstraZeneca. EUROPEAN UNION RISK MANAGEMENT PLAN (EU RMP) FOR VAXZEVRIA (ChAdOx1-S [RECOMBINANT]) [Internet]. 2022 [zitiert 2022 Juni 14];Available from: https://www.ema.europa.eu/en/documents/rmp-summary/vaxzevria-previously-covid-19-vaccineastrazeneca-epar-risk-management-plan_en.pdf
- Burkhardt A, Lang W. Todesursache nach COVID-19-Impfung [Internet]. 2021 [zitiert 2022 Juni 14];Available from: https://www.pathologie-konferenz.de/Tod_nach_COVID-19-Impfung_www_pathologie-konferenz_de.pdf
- Weißer K, Meyer C, Petzold D, Mentzer D, Keller-Stanislawski B. Verdachtsfälle von Impfkomplikationen nach dem Infektionsschutzgesetz und Verdachtsfälle von Nebenwirkungen (von Impfstoffen) nach dem Arzneimittelgesetz vom 1. 1. 2004 bis zum 31. 12. 2005. Bundesgesundheitsbl. 2007;50:1404–17.
- European Medicines Agency. COVID-19 vaccines safety update [Internet]. [zitiert 2022 Juni 14];Available from: https://www.ema.europa.eu/en/documents/covid-19-vaccine-safety-update/covid-19-vaccines-safety-update-12-may-2022_en.pdf
- Tuvali O, Tshori S, Derazne E, Hannuna RR, Afek A, Haberman D, u. a. The Incidence of Myocarditis and Pericarditis in Post COVID-19 Unvaccinated Patients—A Large Population-Based Study. JCM 2022;11:2219.
- Patone M, Mei XW, Handunnetthi L, Dixon S, Zaccardi F, Shankar-Hari M, u. a. Risks of myocarditis, pericarditis, and cardiac arrhythmias associated with COVID-19 vaccination or SARS-CoV-2 infection. Nat Med 2022;28:410–22.
- Gill JR, Tashjian R, Duncanson E. Autopsy Histopathologic Cardiac Findings in Two Adolescents Following the Second COVID-19 Vaccine Dose. Archives of Pathology & Laboratory Medicine [Internet] 2022 [zitiert 2022 Juni 23];Available from: https://meridian.allenpress.com/aplm/article/doi/10.5858/arpa.2021-0435-SA/477788/Autopsy-Histopathologic-Cardiac-Findings-in-Two
- Park DY, An S, Kaur A, Malhotra S, Vij A. Myocarditis after COVID-19 mRNA vaccination: A systematic review of case reports and case series. Clinical Cardiology 2022;clc.23828.
- Meron Grossman S, Schamroth Pravda N, Orvin K, Hamdan A, Vaturi M, Bengal T, u. a. Characterization and long-term outcomes of patients with myocarditis: a retrospective observational study. pwki 2021;17:60–7.
- Ghanizada M, Kristensen SL, Bundgaard H, Rossing K, Sigvardt F, Madelaire C, u. a. Long-term prognosis following hospitalization for acute myocarditis – a matched nationwide cohort study. Scand Cardiovasc J 2021;55:264–9.
- Cirillo N, Doan R. The association between COVID-19 vaccination and Bell’s palsy. The Lancet Infectious Diseases 2022;22:5–6.
- Aleem A, Nadeem AJ. Coronavirus (COVID-19) Vaccine-Induced Immune Thrombotic Thrombocytopenia (VITT) [Internet]. In: StatPearls. Treasure Island (FL): StatPearls Publishing; 2022 [zitiert 2022 Juni 14]. Available from: http://www.ncbi.nlm.nih.gov/books/NBK570605/
- Rote Hand Brief. COVID-19 Vaccine AstraZeneca: Risiko von Thrombozytopenie und Gerinnungsstörungen [Internet]. [zitiert 2022 Juni 14];Available from: https://www.pei.de/SharedDocs/Downloads/DE/newsroom/veroeffentlichungen-arzneimittel/rhb/21-03-23-covid-19-vaccine-astrazeneca.pdf?__blob=publicationFile&v=2
- Mani A, Ojha V. Thromboembolism after COVID-19 Vaccination: A Systematic Review of Such Events in 286 Patients. Annals of Vascular Surgery 2022;S0890509622002199.
- Kim AY, Woo W, Yon DK, Lee SW, Yang JW, Kim JH, u. a. Thrombosis patterns and clinical outcome of COVID-19 vaccine-induced immune thrombotic thrombocytopenia: A Systematic Review and Meta- Analysis. International Journal of Infectious Diseases 2022;119:130–9
- Taquet M, Husain M, Geddes JR, Luciano S, Harrison PJ. Cerebral venous thrombosis and portal vein thrombosis: A retrospective cohort study of 537,913 COVID-19 cases. EClinicalMedicine 2021;39:101061.
- Ab Rahman N, Lim MT, Lee FY, Lee SC, Ramli A, Saharudin SN, u. a. Risk of serious adverse events after the BNT162b2, CoronaVac, and ChAdOx1 vaccines in Malaysia: A self-controlled case series study. Vaccine 2022;S0264410X22007009.
- Greenhawt M, Abrams EM, Shaker M, Chu DK, Khan D, Akin C, u. a. The Risk of Allergic Reaction to SARS-CoV-2 Vaccines and Recommended Evaluation and Management: A Systematic Review, Meta- Analysis, GRADE Assessment, and International Consensus Approach. The Journal of Allergy and Clinical Immunology: In Practice 2021;9:3546–67.
- Klimek L, Eckrich J, Hagemann J, Casper I, Huppertz J. [Allergic reactions to COVID-19 vaccines: evidence and practice-oriented approach]. Internist (Berl) 2021;62:326–32.
- Hertel M, Heiland M, Nahles S, von Laffert M, Mura C, Bourne PE, u. a. Real-world evidence from over one million COVID-19 vaccinations is consistent with reactivation of the varicella-zoster virus. J Eur Acad Dermatol Venereol 2022;
- Dickerman BA, Madenci AL, Gerlovin H, Kurgansky KE, Wise JK, Figueroa Muñiz MJ, u. a. Comparative Safety of BNT162b2 and mRNA-1273 Vaccines in a Nationwide Cohort of US Veterans. JAMA Intern Med [Internet] 2022 [zitiert 2022 Juni 16];Available from: https://jamanetwork.com/journals/jamainternalmedicine/fullarticle/2793236
- Jabagi MJ, Botton J, Bertrand M, Weill A, Farrington P, Zureik M, u. a. Myocardial Infarction, Stroke, and Pulmonary Embolism After BNT162b2 mRNA COVID-19 Vaccine in People Aged 75 Years or Older. JAMA 2022;327:80–2.
- Hazell L, Shakir SAW. Under-reporting of adverse drug reactions : a systematic review. Drug Saf 2006;29:385–96.
- Kassenärztliche Bundesvereinigung. IMPFSTOFFE GEGEN COVID-19: VERGLEICH ANZAHL DER IMPFUNGEN MIT ANZAHL DER CODIERTEN IMPFNEBENWIRKUNGEN 2016-2021 [Internet]. 2022 [zitiert 2022 Juni 27];Available from: https://www.epochtimes.de/assets/uploads/2022/06/2022-06-16_Anfrage-_codierte-Impfnebenwirkungen-Covid-19.pdf
- Paul-Ehrlich-Institut. Sicherheitsbericht COVID-19 Impfung bis 31.12.2021 [Internet]. 2022 [zitiert 2022 Mai 12];Available from: https://www.pei.de/SharedDocs/Downloads/DE/newsroom/dossiers/sicherheitsberichte/sicherheitsbericht-27-12-20-bis-31-12-21.pdf?__blob=publicationFile&v=5
- Autorengruppe „7Argumente“. Anlage 5: Die erhöhte Sterblichkeit im Jahr 2021 [Internet]. 2022 [zitiert 2022 März 17];Available from: https://7argumente.de/anlage-5/
- Statistisches Bundesamt. Sonderauswertung zu Sterbefallzahlen der jahre 2020 bis 2022 – Entwicklung im Jahr 2021 [Internet]. [zitiert 2022 Juni 23];Available from: https://www.destatis.de/DE/Themen/Gesellschaft-Umwelt/Bevoelkerung/Sterbefaelle-Lebenserwartung/sterbefallzahlen.html
- Statista. Anzahl der Lebendgeborenen in Deutschland nach Geschlecht von März 2020 bis März 2022 [Internet]. 2022 [zitiert 2022 Juli 12];Available from: https://de.statista.com/statistik/daten/studie/1247393/umfrage/monatliche-geburtenzahlen-indeutschland-nach-geschlecht/#professional
- Prasad S, Kalafat E, Blakeway H, Townsend R, O’Brien P, Morris E, u. a. Systematic review and metaanalysis of the effectiveness and perinatal outcomes of COVID-19 vaccination in pregnancy. Nat Commun 2022;13:2414.
- Shimabukuro TT, Kim SY, Myers TR, Moro PL, Oduyebo T, Panagiotakopoulos L, u. a. Preliminary Findings of mRNA Covid-19 Vaccine Safety in Pregnant Persons. N Engl J Med 2021;384:2273–82.
- Nafilyan V, Humberstone B, Mehta N, Diamond I, Coupland C, Lorenzi L, u. a. An external validation of the QCovid risk prediction algorithm for risk of mortality from COVID-19 in adults: a national validation cohort study in England. Lancet Digit Health 2021;3:e425–33.
- Guyatt GH, Oxman AD, Vist GE, Kunz R, Falck-Ytter Y, Alonso-Coello P, u. a. GRADE: an emerging consensus on rating quality of evidence and strength of recommendations. BMJ 2008;336:924–6.
- Sackett DL, Rosenberg WMC, Gray JAM, Haynes RB, Richardson WS. Evidence based medicine: what it is and what it isn’t. BMJ 1996;312:71–2.
- Sabnani MK, Rajan R, Rowland B, Mavinkurve V, Wood LM, Gabizon AA, u. a. Liposome promotion of tumor growth is associated with angiogenesis and inhibition of antitumor immune responses. Nanomedicine: Nanotechnology, Biology and Medicine 2015;11:259–62.
- Ndeupen S, Qin Z, Jacobsen S, Bouteau A, Estanbouli H, Igyártó BZ. The mRNA-LNP platform’s lipid nanoparticle component used in preclinical vaccine studies is highly inflammatory. IScience 2021;24:103479.
- Karthik K, Senthilkumar TMA, Udhayavel S, Raj GD. Role of antibody-dependent enhancement (ADE) in the virulence of SARS-CoV-2 and its mitigation strategies for the development of vaccines and immunotherapies to counter COVID-19. Human Vaccines & Immunotherapeutics 2020;16:3055–60.
- Chen Y, Xu Z, Wang P, Li X, Shuai Z, Ye D, u. a. New-onset autoimmune phenomena post-COVID-19 vaccination. Immunology 2022;165:386–401
- Φυσιολογικό κρυολόγημα: Σύμφωνα με νέα μελέτη, η υστερία SARS-CoV-2/COVID-19 πρέπει επιτέλους να σταματήσει https://www.eyewideopen.org/?p=3993
- https://www.eof.gr/c/document_library/get_file?uuid=48702993-6356-43ef-9d88-979064e096fc&groupId=12225
- https://www.eof.gr/web/guest/home;jsessionid=6887f5b337cc13578ffd18d5a775?p_p_id=62_INSTANCE_2QyB&p_p_lifecycle=0&p_p_state=maximized&p_p_mode=view&_62_INSTANCE_2QyB_struts_action=%2Fjournal_articles%2Fview&_62_INSTANCE_2QyB_groupId=12225&_62_INSTANCE_2QyB_articleId=17508&_62_INSTANCE_2QyB_version=1.0
- Σύγχυση με τα δεδομένα του ΕΜΑ, ο ΕΟΦ αμφισβητεί το θάνατο ανηλίκου στην Ελλάδα https://www.eyewideopen.org/?p=3732
- Ανάλυση των δεδομένων της επιδημίας COVID-19: τι σκοτώνει τελικά τους Έλληνες; https://www.eyewideopen.org/?p=3466
Hμερομηνία δημοσίευσης: 04.08.2022
Follow us: